香港大學李嘉誠醫學院(港大醫學院)微生物學系的研究人員發現會加速感染SARS-CoV-2 及Omicron變異株的新型宿主蛋白酶,為對應新冠大流行提供了新方向。除了新型宿主蛋白酶,研究團隊發現細胞膜上的膜型基質金屬蛋白酶(MT-MMP)及去整合素金屬蛋白酶(ADAM),作為入侵細胞的中介,亦能引導SARS-CoV-2入侵,同時提升應對Omicron BA.1的效率。此發現以抑制MMP來有效對應Omicron BA. 1及其變種的綜合治療提供了新研究策略。研究成果現已發表在國際科學期刊《Science Advances》(按此瀏覽期刊文章)。
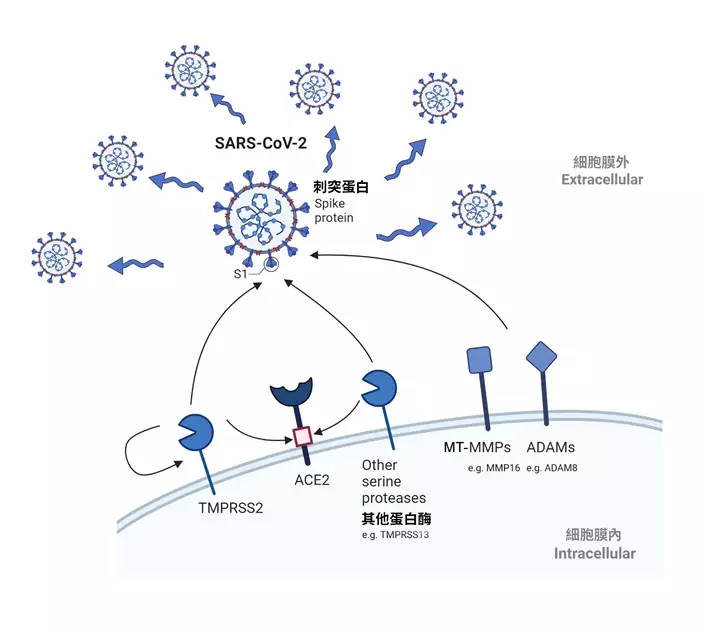
MT-MMPs能夠切割 SARS-CoV-2 的刺突蛋白及ACE2的受體蛋白,促進刺突蛋白介導的合胞體形成,加速SARS-CoV-2的感染。
背景
SARS-CoV-2在人與人之間的傳播力極高。過去三年,SARS-CoV-2在二百個國家或地區累計超過6.5億宗病例,超過668萬宗死亡病例。1 SARS-CoV-2在入侵細胞的過程中需要利用宿主蛋白酶切割病毒的刺突蛋白。除了TMPRSS2,最近有證據表明其他蛋白酶包括TMPRSS4、TMPRSS11D和TMPRSS13同樣可以激活細胞膜上的SARS-COV-2刺突蛋白,惟其原因仍未完全清楚。因此,探究宿主蛋白酶在促進 SARS-CoV-2 入侵細胞中的作用,有助了解SARS-CoV-2感染與發病機制,是一個重要的研究課題,亦能為治療COVID-19提供新方向。
研究方法和結果
通過使用假病毒篩選系統,團隊發現細胞膜上的MT-MMP及ADAM能夠加速SARS-CoV-2入侵細胞。研究人員隨後採用體外及體內模型實驗,評估 MT-MMP 介導的 SARS-CoV-2 入侵細胞的生理重要性:在細胞模型中,發現MMP 抑制劑在人肺及腸細胞中的 SARS-CoV-2複製率分別減少了 96% (p < 0.0001) 和 85% (p <0.0001),可見抑制宿主MT-MMP可顯著降低SARS-CoV-2的入侵及複製,顯示抑制MT-MMP可有助對抗 SARS-CoV-2。
在倉鼠模型中, MMP 抑制劑顯著降低了 SARS-CoV-2 的肺部病毒載量(p < 0.0001),並減輕倉鼠肺部組織的損傷。研究團隊在倉鼠的鼻甲和肺部中,發現與SARS-CoV-2原始株相比,MT-MMP 對應SARS-CoV-2 Omicron BA.1的效果更好。而且在抑制病毒複製方面較MMP 抑制劑絲氨酸蛋白酶抑制劑(camostat)更加有效。研究團隊也證實了 MT-MMP在機制上能夠切割 SARS-CoV-2 的刺突蛋白(S)及一種稱為血管緊張素轉化酶2(ACE2)的受體蛋白,促進刺突蛋白介導的合胞體形成,由此來加速SARS-CoV-2的感染。這些研究成果揭示了其他新型蛋白酶對於 SARS-CoV-2 入侵的影響,加深對SARS-CoV-2感染和發病機制的了解。
研究意義
港大醫學院臨床醫學學院微生物學系臨床副教授陳福和醫生表示:「此研究揭示了 SARS-CoV-2 原始株及 Omicron 變異株感染過程中利用的新型膜蛋白酶,有助了解冠狀病毒的入侵機制。此外,這些發現對於研發針對Omicron變異株的藥物非常重要。」
研究團隊
是次研究由港大醫學院臨床醫學學院微生物學系助理教授朱軒博士及臨床副教授陳福和醫生領導。













