是項研究為定義高效幹細胞的「家」邁出了重要的一步。
香港大學李嘉誠醫學院(港大醫學院)一項最新研究確定了第四型膠原蛋白──一種細胞外基質蛋白(ECM)──在具有再生能力的扁蟲(渦蟲)裡有調控多功能幹細胞的作用。第四型膠原蛋白在渦蟲中是調控幹細胞如何分裂或演變的重要一環,也是渦蟲能再生組織的關鍵。是次研究成果有助加深對人類組織再生潛能的理解。

香港大學。資料圖片
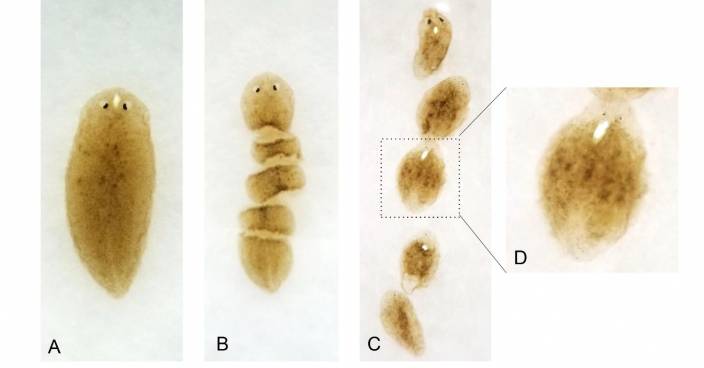
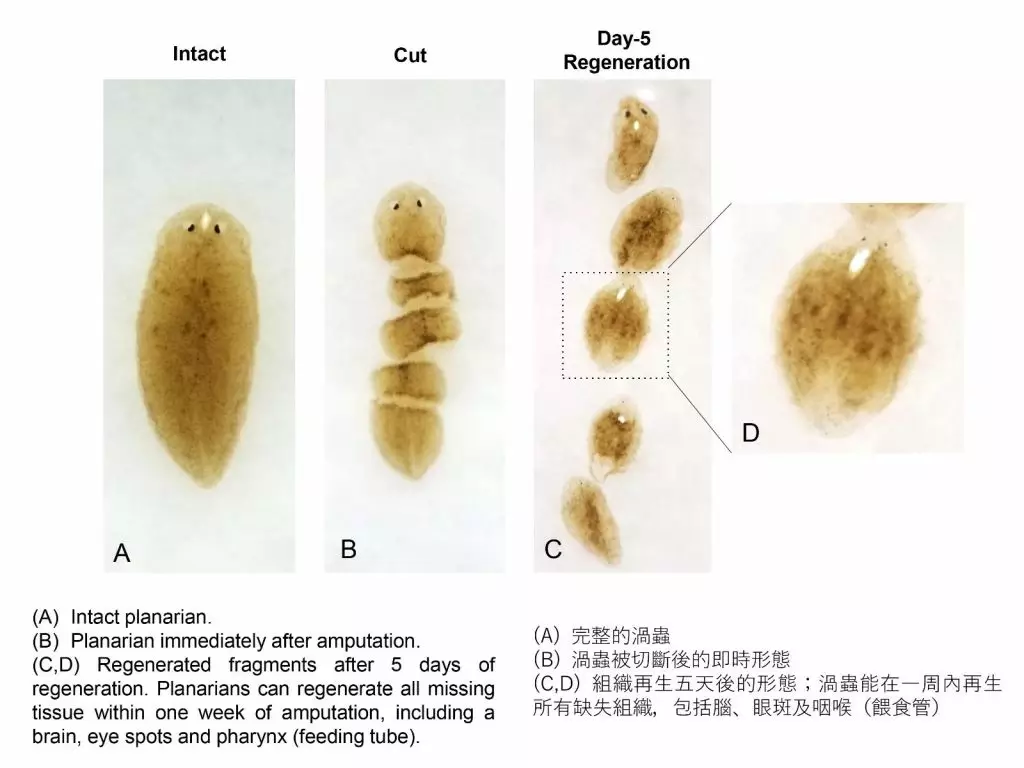
渦蟲的成蟲在成長過程中能保存大量(約三成)的高效幹細胞,如有任何組織缺失,甚至斷頭後,也能再生組織,讓大腦重生。渦蟲為何能保存大量高效幹細胞,至今仍是未解的謎團;但過去一個多世紀以來,生物學家為此著迷不已。
所有幹細胞都有一個由不同類型的細胞外基質蛋白(包括膠原蛋白)組成、被稱為「生態位」的「家」。這個「家」會發出不同的信號,指示幹細胞運作。細胞外基質蛋白是構建幹細胞周遭環境的基礎──其中第四型膠原蛋白是非常原始的細胞外基質成分,存在於上皮組織之間的基底膜,哺乳類動物在演化過程中亦保存了相似的結構或序列。
港大醫學院生物醫學學院的研究團隊在是次研究發現,第四型膠原蛋白作為渦蟲幹細胞生態位的關鍵組成部分,如何參與調控利用幹細胞的方式,使缺失組織重生的機制。因為細胞外基質是構建幹細胞周遭環境的基礎,第四型膠原蛋白就是基質其中一種成分。是項研究為定義高效幹細胞的「家」邁出了重要的一步。
是項研究發現,移除渦蟲體內的第四型膠原蛋白將能導致幹細胞加速分裂,但分裂出來的細胞卻失去成為其他組織類型細胞的能力,以致組織破裂而非再生。研究團隊進一步帶出第四型膠原蛋白與一個分子途徑的關聯,該分子途徑涉及由神經元產生的生長因子Nrg-7,而Nrg-7會刺激幹細胞增殖,在移除第四型膠原蛋白後效果更會加強。然而,這些增殖出來的幹細胞始終無法變成其他類型的細胞,以修護或保留渦蟲的組織。
儘管人類的組織和器官在日常損耗或輕度損傷後,可以通過成體的幹細胞來修復,但是人類在嚴重損傷的情況下,卻無法自我修復或再生。要展開這自我修復或再生過程,將需要在合適的環境下使用更高效的幹細胞。然而, 目前對於人類組織和器官再生的認知仍然有限,透過了解渦蟲如何利用第四型膠原蛋白,例如渦蟲的成蟲能保留三成幹細胞這種哺乳類動物無法達成的事,將有助解構在人類實踐組織再生的奧秘。

香港大學。資料圖片
領導是項研究的港大醫學院助理院長(研究生課程)、生物醫學學院教授、鄭兆如鄭杏如基金教授(幹細胞生物學及再生醫學)陳振勝教授表示:「能在刀下不朽的生物深深吸引作為科學家的我,令我更震驚的是渦蟲被切成幾份後仍能生存,甚至保存很多幹細胞,並再生成另一條渦蟲的能力,啟發了我們的研究──渦蟲成蟲在含細胞外基質蛋白的環境下仍能保存很多幹細胞,這一步非常重要,為人類重建缺失組織帶來希望。身為骨骼生物學家,我期望有一天可以看到人類重新長出失去了的身體部分。」

香港大學。資料圖片
發掘人類再生缺失組織的潛力,是一個引人入勝的夢想,透過了解如渦蟲等生物怎樣重生其缺失的組織,將有助推動在哺乳類動物身上進行相關研究。日後有關再生動物如渦蟲身上的細胞外基質蛋白的研究,將加深人類對這方面的認識,並以此為基礎,嘗試為人類幹細胞建造生態位。其中一項長遠目標是於建造能儲存大量人類幹細胞的人造生態位,以應用於受損部位,協助缺失組織再生。