產品是用於治療胃部疾病的處方藥物
衞生署表示,同意持牌藥物批發商顯榮行自願回收一款含有雷尼替丁的產品,即「Epadoren 50毫克/2毫升注射液」(香港註冊編號:HK-61752),因為可能含有雜質。
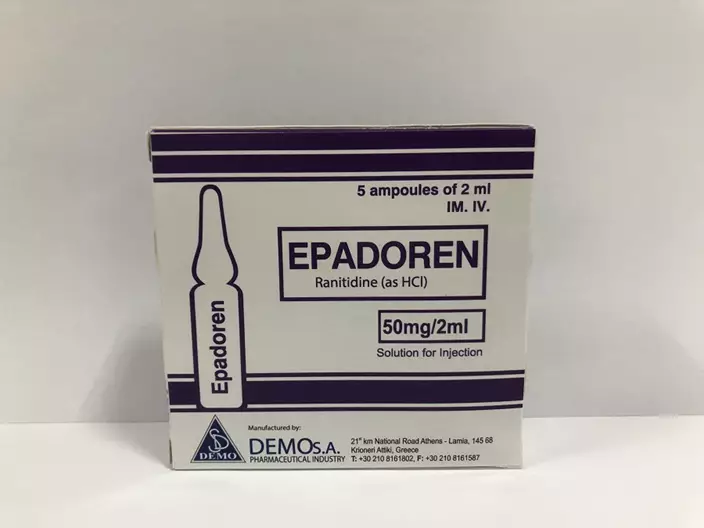
圖示Epadoren 50毫克/2毫升注射液。政府新聞處圖片
衞生署今日接獲顯榮行通知,指有關產品的製造商基於近期就有關雜質的外地報道,故懷疑上述產品可能含有雜質N-亞硝基二甲胺(NDMA)。基於實驗室測試,NDMA被列為可能令人類患癌的物質。作為預防措施,顯榮行自願從市面回收受影響的產品。
衞生署得悉一些含有雷尼替丁的產品在外國被發現含有NDMA,並自9月24日起先後共批准了7款含有雷尼替丁產品的自願回收。衞生署正繼續從市面上抽取含有雷尼替丁產品樣本作檢驗。衞生署亦得悉海外藥物監管機構正評估含有雷尼替丁產品被發現含雜質對安全性的影響。署方會密切監察事件的發展和海外藥物監管局就該藥物發出更新的安全評估,以考慮任何必要的跟進行動。衞生署亦已於9月18日發信予醫護人員,通知他們有關事件。
上述產品是用於治療胃部疾病的處方藥物。根據顯榮行的資料,受影響產品曾供應予私家醫院、本地醫生、獸醫和藥房。顯榮行已設立熱線電話(2541 5731)解答相關查詢。衞生署至今未有接獲涉及有關產品的不良反應報告,並會密切監察有關回收。


