港大醫學院和廣州中山大學中山眼科中心的研究團隊合作,成功研發新型光活化聯合療法,用於治療老年黃斑病變。
此新療法通過靜脈注射納米製劑,並向患者眼睛進行光照,以激活抗血管增生和光動力聯合療法,為治療黃斑病變和其他由異常血管增生所引致的眼疾提供新的微創治療方案。研究成果現已在國際學術期刊《Advanced Science》發表,並已根據專利合作條約提出國際申請。
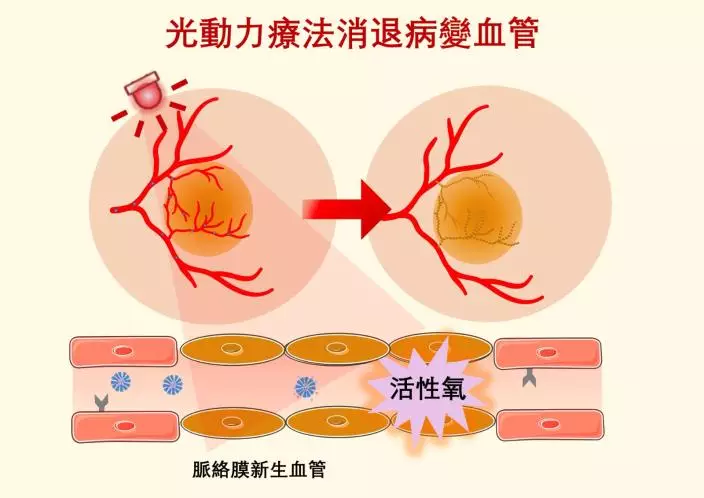
光動力療法提供一種臨床解決方案,利用特定波長的光照激活無毒光敏藥物,產生活性氧,從而破壞和清除病變血管。
根據香港眼科調查2019年發表的數據,早期老年黃斑病變在本港70歲以上人口中發生率高達7.5%1,是導致香港成年人視力障礙及失明的第二大病因。目前,在眼內玻璃體注射抗血管內皮生長因子是治療濕性黃斑病變的首選方案。然而,這種侵入性的治療方式可能引起病人不適,並可能伴隨嚴重的併發症風險,如眼內炎和視網膜剝離等,因此有迫切需要開發一種非眼內注射方式,如靜脈注射,實現眼內遞送抗血管增生藥物的製劑技術。
此外,傳統的抗血管增生藥物在清除現有增生血管的效果欠佳。光動力療法提供一種臨床解決方案,利用特定波長的光照激活無毒光敏藥物,產生活性氧,從而破壞和清除病變血管。目前,光動力療法已廣泛應用於治療息肉狀脈絡膜血管病,這是亞洲區濕性黃斑病變的常見類型。因此,結合抗血管增生療法和光動力治療可為濕性黃斑病變的治療提供更有效的方案,有助延緩病情惡化,同時改善患者視力。
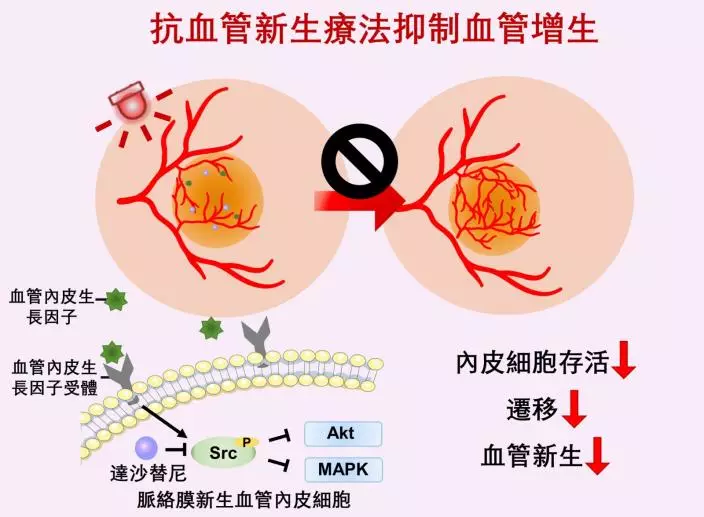
抗血管增生療法通過壓抑與血管內皮生長因子(VEGF)相關的路徑,抑制脈絡膜新生血管形成(CNV)。這項研究首次將抗血管增生藥物和光敏藥物結合製成納米製劑用於黃斑病變治療,為黃斑病變和其他新生血管性眼病的微創療法提供了新的方向。
研究團隊設計了新型光活化納米藥物,將納米藥物單次靜脈注射在有脈絡膜增生血管的小鼠模型,然後對小鼠的眼部進行紅光輻照,以激活納米製劑中的光敏藥物並產生活性氧,這種活性氧不僅促使眼部病變血管消退,同時觸發抗血管增生藥物從納米製劑中釋放,抑制病變血管繼續增生。研究結果顯示,該聯合療法效果顯著,而且沒有導致明顯的全身或眼部的副作用。
這項研究首次將光活化抗血管增生藥物與光敏藥物結合製成納米製劑用於黃斑病變治療,治療程序既簡單又安全。通過靜脈注射和眼部光照,抗血管增生藥物和光敏藥物可發揮聯合效應。這一創新成果為黃斑病變和其他新生血管性眼病的微創療法提供了新的方向。此外,這項研究採用美國食品藥物管理局(FDA)批准的藥物和藥用輔料進行製劑設計,或有助將來的臨床轉化。

港大醫學院團隊研發光活化聯合療法,用於治療老年黃斑病變。 研究團隊成員包括(左起):李嘉博士、許舒婷、汪衛平博士、樊妮博士與龍凱麒。
香港大學李嘉誠醫學院(港大醫學院)公共衞生學院研究團隊發現,每周僅進行一次間歇快步運動,已能有效幫助中央肥胖人士顯著減少身體脂肪並提升心肺功能,其效果與傳統建議的每周進行三次間歇運動相若。這項研究提供了有力的科學證據,證實每周一次的間歇快步運動可作為肥胖人士的運動治療方案,尤其適合運動時間有限的人士。該研究成果已於國際學術期刊《自然通訊》發表。

蕭明輝教授(中)表示,雖然每周三次的間歇訓練是治療過度肥胖的常見方案,但研究結果證實每周一次總時數相同的間歇訓練亦可達致相近成效,可成為繁忙人士的有效運動替代方案。
科學實證運動方案 有效改善肥胖
肥胖是一種常見的慢性疾病,特徵為體內脂肪過度積聚,進而損害健康。尤其是集中於腹部位置的中央型肥胖,會增加患上心血管疾病、代謝失調,甚至死亡風險。恆常運動雖然對健康有益,亦是肥胖管理的重要一環,然而長期維持運動習慣對許多人來説並不容易,對肥胖人士尤為困難。
間歇訓練是指交替進行高強度與低強度的動態恢復運動。相較傳統的持續中等強度運動,間歇訓練能更有效省時地減少全身及內臟脂肪。然而,現時的標準運動指引通常建議每周進行三次間歇訓練,對於時間有限和缺乏運動空間的人士而言,實在難以實行。過往研究發現,將每周運動量集中於一至兩天進行的「周末戰士」運動模式具有正面效果,但以此模式進行間歇訓練的成效,目前仍缺乏充分的科學佐證。
港大醫學院公共衞生學院運動學分部主任兼教授蕭明輝教授強調,驗證每周一次與每周三次間歇訓練的成效是否相若十分重要,藉此能提供一個具科學依據的替代運動方案。

港大醫學院研究發現,在總運動時數相同的情況下,每周進行「間歇快走」可顯著減脂及提升心肺功能,效果與傳統建議的每周進行三次間歇運動相若。
運動頻率減少 健康成效相近
2021年9月至2024年9月期間,港大醫學院的研究人員在本港進行了一項嚴謹的測試,對象為315名18歲或以上、超重且患有中央肥胖的華人。參與者被隨機分為三組,分別為每周一次間歇訓練組、每周三次間歇訓練組,以及對照組。
在為期四個月的研究期間,對照組每兩周參加一次2.5小時的健康教育課程;另外兩個間歇訓練組則每周進行合共75分鐘的間歇訓練,參加者可選擇一次完成或分三次進行。研究於三個時間點透過雙能量X光吸收儀測量參加者的體脂量,分別是幹預前、幹預後第16周,以及第32周(即幹預後四個月)。
試驗結果顯示,在第16周評估階段,不論每周一次或三次的間歇訓練均能有效減少多餘體脂。以全身脂肪量、體脂率及腰圍等指標衡量,兩組改善幅度相近,且與對照組相比,兩種訓練模式均能提升心肺功能。
蕭明輝教授表示:「雖然每周三次的間歇訓練仍是治療過度肥胖的常見方案,但我們的研究結果證實每周一次間歇訓練亦可達致相近的成效,可作為實用的運動策略。對於需兼顧工作、學業、家庭及其他事務的人士而言,時間限制是難以每周維持多次運動的主要障礙。」他補充,其實無需依賴高頻率運動,每周一次的間歇訓練同樣是可行且有效的替代方案。














