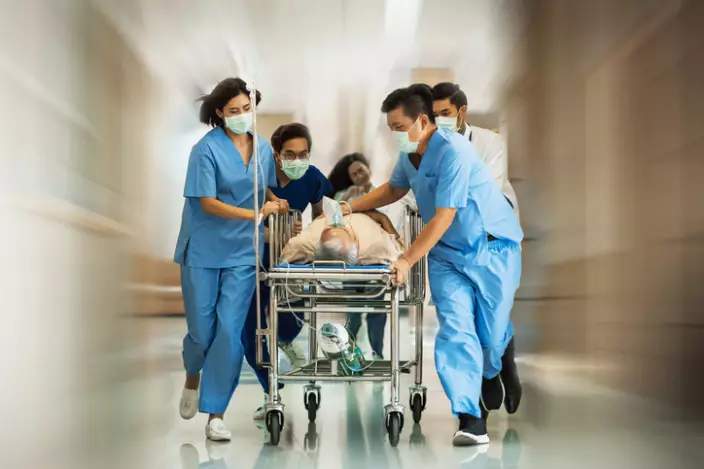
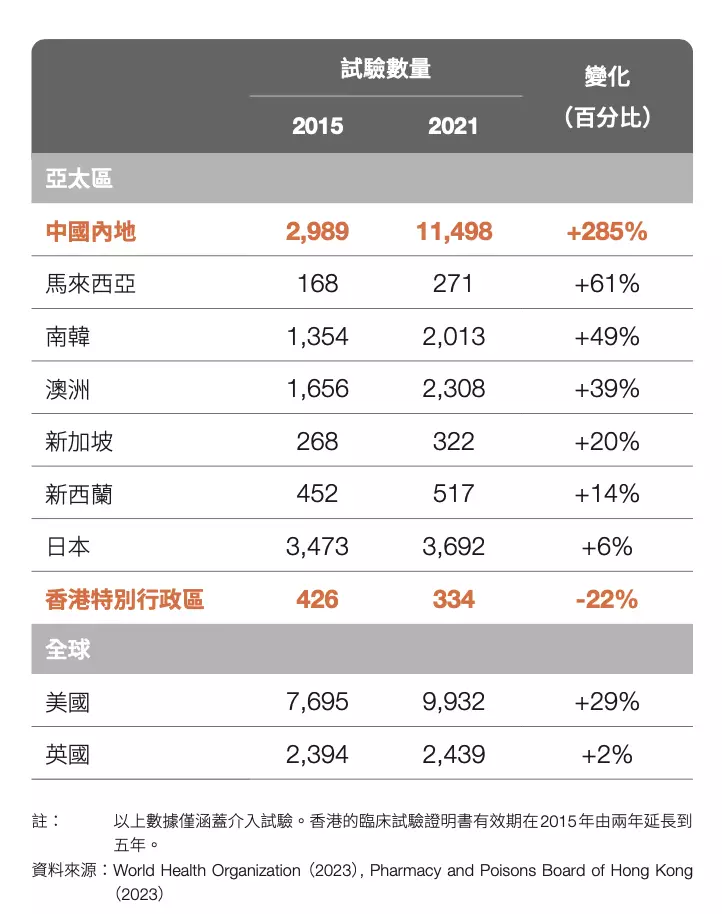
本港臨床試驗數量於2021年只有334宗,較2015年減少22%,但同期鄰近地區卻有明顯升幅。團結香港基金發表研究書,建議增強本港臨床研究能力,充分發揮香港藥物樞紐角色。

團結香港基金發表新一份題為《凝聚政產學研力量 建設臨床研究之都》的政策倡議,指臨床研究是生物科技價值鏈之中的關鍵一環,不但能彌合香港學術研究與藥物商業化之間的鴻溝,更能吸引製藥公司入駐新藥研發基地,讓患者從最新臨床創新突破中獲益。

設計圖片
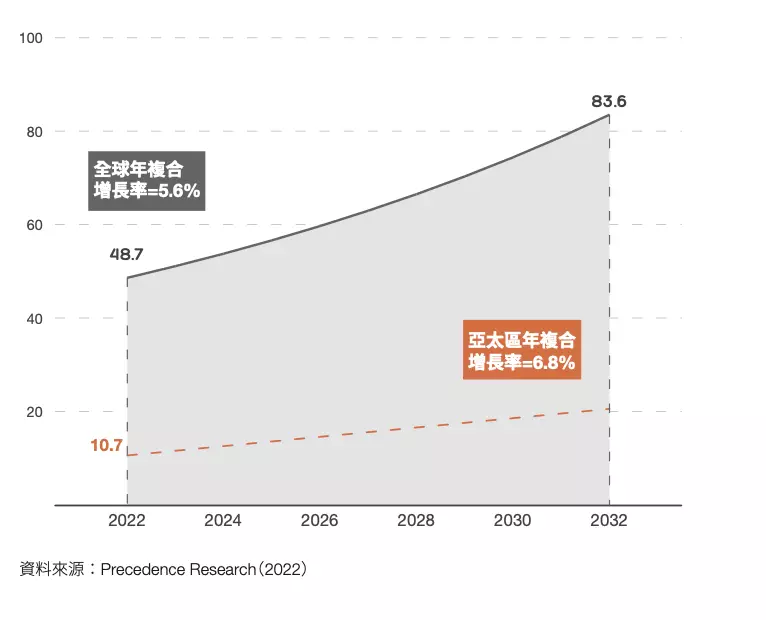
由英國國家健康與保健研究所的經驗可見,針對臨床試驗的投資可產生高達 7.6 倍的經濟效益,足以顯示其經濟發展潛力。未來十年,全球的臨床研究試驗預計將以每年 6%的速度快速增長,亞洲將成為其中主要引擎。然而,香港的臨床試驗數目在2015至2021年間卻下降了 22%,與主要經濟體平均 48%的增長, 以至內地 285%的爆發式增長形成鮮明對比。
報告指香港臨床研究主要面臨的三方面挑戰。首先,臨床研究者及研究輔助人員缺乏支持; 其次相對於周邊的經濟體,香港批核臨床試驗及簽訂合同的流程過長且累贅。其三,香港並無進行第一 層藥物審查的能力,即審查臨床試驗數據以批准藥物註冊的能力,藥物需先經過外地審批再來港進行第二層審查, 大大降低了他們在香港進行臨床試驗的意願。
報告提出五項建議,包括透過招商引資、培養人才,增強香港作為中西橋樑的地位,從而將香港建設為臨床研究及藥品商業化的首選地。其中重點包括成立臨床研究所推動政策落實,以及設立香港獨立的藥物第一層審查機構。
對於施政報告提出「1+」藥物審批機制,罕見病及癌症新藥只需一個地區的認可書、以及本地的專家審核即可註冊。團結香港基金表示,需確保「1+」機制審批時間不應長於原本機制。另外,第二層審批機制亦可望加快,期望香港於2030年可全面審批藥物。