由香港大學李嘉誠醫學院臨床醫學學院教授楊偉國和醫生陳福和共同領導的研究團隊發現,感染嚴重急性呼吸綜合症冠狀病毒2 (SARS-CoV-2)可誘發破骨細胞的炎性,在患上急性冠狀病毒病(COVID-19)及康復後期造成嚴重的骨質流失。是項研究為新冠肺炎在骨骼系統上的長期併發症提供新見解。相關研究結果已在國際學術期刊《自然通訊》發表。

香港大學李嘉誠醫學院。資料圖片
目前對於感染新冠病毒引致的臨床症狀,特別是對骨組織代謝的影響,尚缺全面的了解。為了研究新冠病毒對骨組織代謝的影響,研究團隊在敘利亞倉鼠模型鼻內注入新冠病毒,並收集牠們受感染後的骨組織樣本。通過三維微米級計算機斷層成像技術,團隊發現感染新冠病毒會引起長骨及椎骨等部位內的小梁骨結構,出現20%至50%不等的嚴重骨質流失。急性感染所引起的骨質流失,更會持續較長時間。研究進一步發現骨質流失與因感染新冠病毒誘導的細胞因子失調有密切關係。這種病理上的骨質缺乏與破骨細胞(一種負責骨組織吸收的細胞)的炎性息息相關;由感染新冠病毒引起的細胞因子失調不單影響破骨細胞分化,而且還在骨骼組織中引起促炎症反應,增強其促進破骨細胞生長的影響。
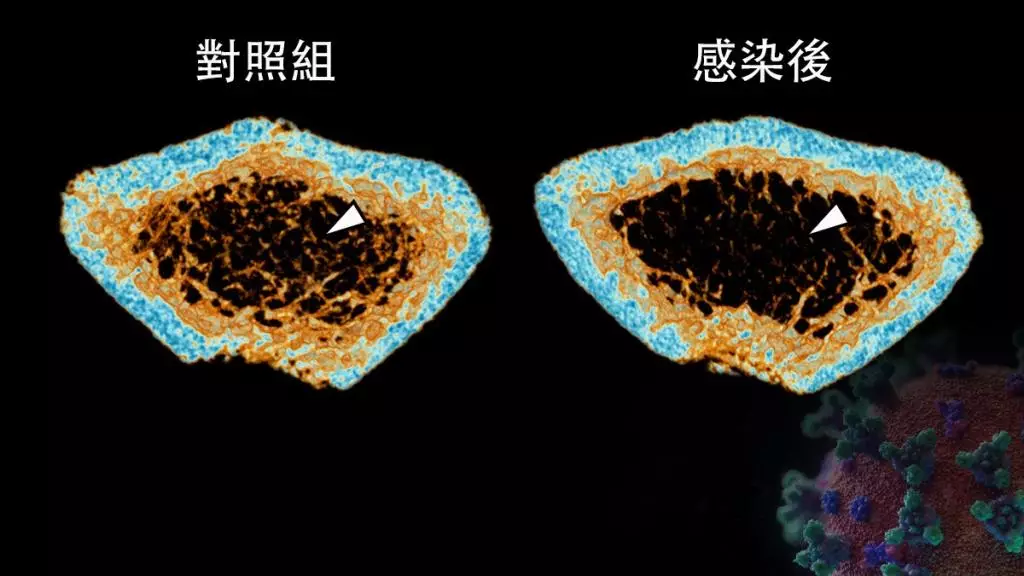
港大圖片
是項研究是全球首次利用接近人類感染新冠病毒狀況的敘利亞倉鼠模型,研究新冠病毒對骨組織代謝的影響。研究結果證明,新冠病毒引發的病理性骨質流失可能是一種被忽視的併發症,未來需要在 COVID-19患者的後續跟進中更廣泛調查相關情況。

陳福和。資料圖片

網圖











