生於香港這個物質豐富的社會,又身為家中唯一的「小公主」,當然萬千寵愛在一身。正當擔心「小公主」會否被寵壞之際,家中傳來好消息,就是「小公主」快要當上姊姊了,而我和丈夫亦一直希望這個身份能幫助「小公主」戒除「公主病」。

姊姊陪弟弟練習抬起頭
家中快要添一名新成員,當然要盡快通知這位在家裏地位舉足輕重的「小公主」。我思前想後,很感恩上帝給了我靈感。我對「小公主」說﹕「Jocelyn,因為天父爸爸說你很乖,希望獎勵你,所以送一個弟弟給你。」「小公主」聽罷十分雀躍說﹕「媽咪,好嘢!我就快當上姊姊!這是我的禮物。」對於姊姊這個身份她十分受落。對媽媽來說,擔心「小公主」吃醋的第一關算是順利通過。
餘下的十個月,爸媽要好好為她做好「心理輔導」,幫助她享受擔任姊姊這個角色。這十個月來,這個三歲多的「小公主」成熟了不少,還懂得保護媽媽。每次見到同學或老師,她都會興奮地介紹說﹕「這是我的媽媽,我媽媽大肚,我快要有個小弟弟。」閒時若遇上一些「橫衝直撞」的小孩,她會著緊地說﹕「我媽媽大肚,小心不要撞到媽媽。」
弟弟出生的日子到了。為免因過份著緊弟弟而忽略姊姊,又希望姊姊對弟弟留下美好的第一印象。爸爸帶姊姊到醫院探望媽媽和弟弟,讓她分享喜悅;而媽媽在入院前亦已預先為弟弟準備了一份禮物送給姊姊。弟弟第一天回家,媽媽便代他把這份禮物送給姊姊。
現在小弟弟Jeremy已經五個多月了,姊姊從沒吃醋,還會為弟弟每一個成長重要階段打氣。她會示範動作,讓弟弟學習抬起頭和轉身;看見弟弟成功,姊姊會為他興奮歡呼。平日蹦蹦跳跳地入教室上數學課的姊姊,試過一、兩堂不願上課。但有弟弟送姊姊到教室,姊姊即時充滿能量,再度愛上學習。看到姊弟情深的情景,當媽媽的怎會不窩心。此刻的心願是他們能在成長至到老的階段也能互相扶持。
J&J 媽咪
** 博客文章文責自負,不代表本公司立場 **
日本研究團隊發現新型天然抗癌細菌,單次治療令腫瘤完全消退,療效遠勝現有療法。
日本研究團隊發現新型天然抗癌細菌,單次治療令腫瘤完全消退。資料圖片
研究取得突破 單次治療腫瘤完全消退
近日,日本科研團隊在癌症治療研究方面取得突破性進展,發現一種具高度抗癌潛力的腸道細菌,單次治療即可令腫瘤完全消退。相關研究由日本先進科學技術大學院大學主導,成果已刊登於國際學術期刊Gut Microbes。

日本研究團隊發現新型天然抗癌細菌,單次治療令腫瘤完全消退。資料圖片
來自兩棲爬行類腸道 鎖定關鍵菌株
研究團隊將研究焦點放在兩棲類及爬行類動物的腸道微生物群,從日本樹蛙、紅腹蠑螈及草蜥體內分離出9種細菌菌株。其中,一種名為Ewingella americana(美洲伊麗莎菌)的細菌,在動物實驗中展現出前所未有的抗腫瘤效果。研究顯示,該菌株經過單次靜脈注射後,在結腸癌小鼠模型中達到100%腫瘤完全消退率,療效明顯優於現有免疫治療及化療藥物。
雙重抗癌機制 直接殺癌兼啟動免疫
研究指出,E. americana 具備「雙重抗癌機制」。一方面,該細菌可直接分泌具細胞毒性的物質,破壞腫瘤細胞。另一方面,也能激活體內多種免疫細胞,包括T細胞、B細胞及中性粒細胞,形成協同免疫反應。在對照實驗中,使用抗 PD-L1 抗體或脂質體阿霉素的組別,完全緩解個案極少甚至未見,而 E. americana 則在同一模型下實現全面腫瘤清除。

日本研究團隊發現新型天然抗癌細菌,單次治療令腫瘤完全消退。資料圖片
精準鎖定腫瘤 靶向效率大幅提升
作為兼性厭氧菌,E. americana能憑藉腫瘤組織低氧的微環境特性,實現高度精準的腫瘤定位。實驗結果顯示,靜脈注射後3小時內,該菌株於腫瘤部位的濃度可上升至正常組織的約3000倍,而在其他主要器官中則幾乎無法檢測。研究認為,這種選擇性定植與腫瘤組織中異常血管結構、壞死區域以及抑制免疫清除的生物訊號有關,腫瘤靶向效率較傳統化療藥物高出約40倍。
快速啟動免疫反應 建立長期免疫記憶
在免疫反應層面,E. americana並非僅透過解除免疫抑制發揮作用,而是透過病原體相關分子模式(PAMPs)刺激體內 TLR/NLR 受體,啟動連鎖免疫反應。治療後短短6小時內,中性粒細胞已大量滲入腫瘤組織,並伴隨IFN-γ及TNF-α等發炎因子釋放,最終引發廣泛腫瘤細胞凋亡。值得注意的是,治癒後的小鼠在60日後再次接受腫瘤挑戰時,仍展現完全免疫反應,顯示該療法可建立持久的免疫記憶。
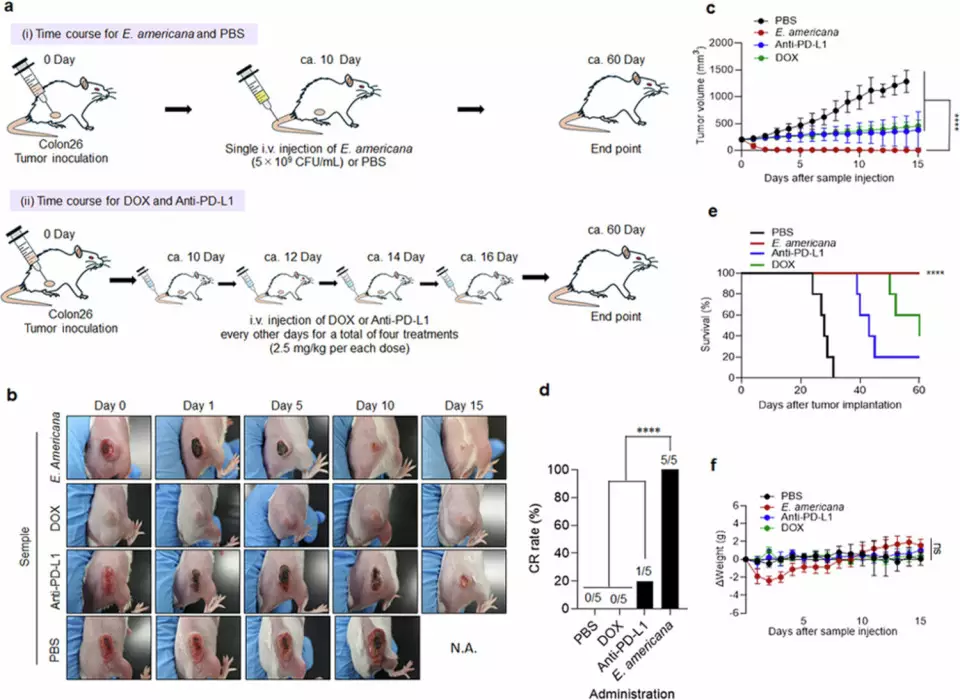
日本研究團隊發現新型天然抗癌細菌,單次治療令腫瘤完全消退。網上圖片
安全性評估理想 可控風險較低
安全性方面,研究結果同樣令人關注。在高達 5×10⁹ CFU/mL 的劑量下,實驗動物的體重變化控制在合理範圍內,血液生化指標及主要器官組織均未見明顯異常。研究指出,與基因改造細菌相比,天然來源的E. americana具有較低突變風險,且在血液中可於24小時內被完全清除,同時仍能在腫瘤組織中維持作用。若出現菌血症,也可透過常規抗生素有效控制。
開拓「活體藥物」概念 臨床轉化前景可期
研究團隊表示,該發現為癌症治療提供多項重要啟示。首先,低等脊椎動物的腸道微生物或是一個尚未充分開發的抗癌資源,目前團隊已建立包含45種菌株的研究庫。其次,「活體藥物」的概念有望突破傳統藥物在腫瘤內濃度不足的限制,透過自我增殖維持療效。此外,由於該菌株屬天然來源,或可避開部分合成生物學相關的監管障礙,臨床轉化時間有望縮短至3至5年。
應用前景擴展 或惠及免疫治療無效患者
儘管目前研究仍以皮下腫瘤模型為主,團隊認為對轉移性腫瘤的應用潛力值得進一步探索。研究人員也正開發口服劑型,透過腸溶包衣技術提升胃酸耐受性,期望為結直腸癌及肝轉移癌帶來新的治療選項。尤其值得關注的是,E. americana對「冷腫瘤」(免疫細胞滲入不足的腫瘤)可能具有療效,或為現有 PD-1/PD-L1 治療無反應患者提供新希望。
生物多樣性具醫學價值 自然界或藏更多解方
研究團隊指出,此項研究不僅為微生物抗癌研究開拓新方向,也突顯生物多樣性保育在醫學發展中的潛在價值。隨著宏基因組測序及類器官培養技術持續進步,來自自然界的「活體藥物」或將為癌症治療帶來更多突破。















