由香港大學(港大)領導的國際團隊取得突破性發現,首次在哺乳動物中發現及證實一種名為ANKLE1的人類蛋白質,能夠感應並回應DNA物理張力的DNA切割酶(核酸酶)。這種「張力感應」機制在細胞分裂過程中維持遺傳物質完整性至關重要;該機制失常可能導致癌症等嚴重疾病。
這項研究結果已經發表在《自然-通訊(Nature Communications)》,象徵着科學家在理解細胞保護自身DNA機制方面的重大進展。研究由港大生物科學學院陳英偉教授團隊與深圳灣實驗室(Shenzhen Bay Laboratory, SZBL)Artem Efremov博士團隊跨領域合作完成;並獲香港科技大學及倫敦弗朗西斯·克里克研究所(Francis Crick Institute in London)的科學家參與。
DNA承受壓力:細胞分裂過程中的隱藏危機
每當細胞分裂時,DNA都要被精準複製並平均分配到兩個新細胞。然而,此過程並非每次都能順利進行——有時DNA會纏結,形成「染色質橋」——這些DNA絲狀結構在細胞分裂過程中連接着兩個新細胞,並承受着強烈的物理張力。若這些橋梁以不受控制的方式斷裂,便可能引發嚴重的基因錯誤,導致癌症或免疫疾病。
研究通訊作者陳英偉教授解釋:「可以把細胞分裂時出現的染色質橋想像成被拉緊的繩索。如果它們突然斷裂,便會對基因組造成嚴重損害,導致突變和不穩定。」在此之前,科學家尚未完全了解細胞如何能在不造成災難性損害的情況下,安全解決這些承受張力的DNA橋。
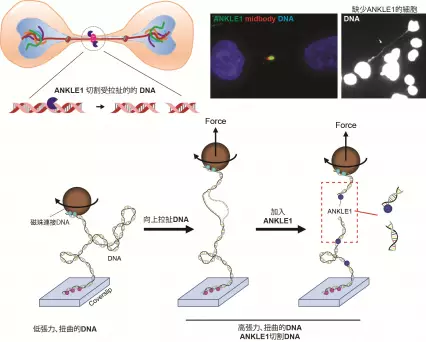
港大與深圳灣實驗室科學家發現首個具「張力感應」的人類DNA切割酶 揭示細胞預防遺傳疾病的新機制
ANKLE1:基因組首個「張力感應」DNA切割酶
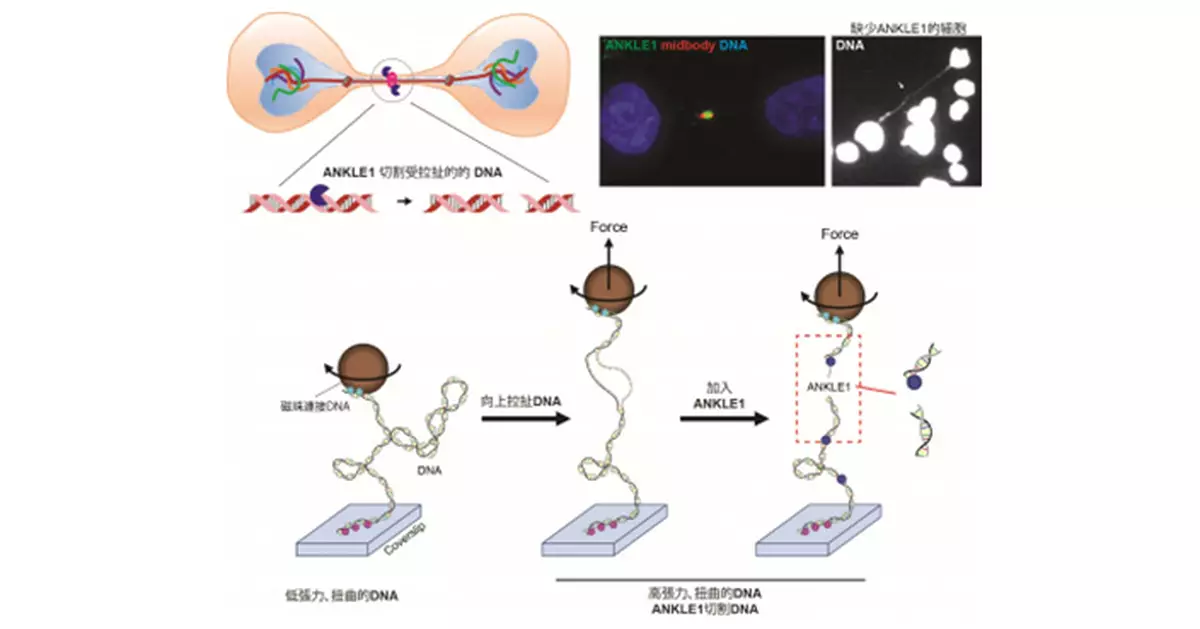
研究揭示,原本已知與DNA修復相關的蛋白質ANKLE1,其實在細胞分裂過程中扮演着一種具「張力感應」的核酸酶。研究團隊運用先進的單分子實驗技術——以微型磁鉗操控單條DNA分子——發現ANKLE1能夠「感受」DNA的拉伸或扭曲,並只會切割處於張力或超螺旋(扭曲)狀態的DNA,就如同被過度拉緊的染色質橋一樣。這種精確性機制防止了DNA隨機斷裂,維持基因組穩定。
共同通訊作者、生物物理學專家Efremov博士表示:「我們的研究顯示,ANKLE1就像一把智能剪刀,只會在必要時——當DNA受拉伸、處於危險之際才會進行切割。這是一種細胞感應並回應基因物理壓力的全新機制。」
團隊結合傳統生物學與尖端生物物理技術,對DNA分子施加精確力量,並實時觀察ANKLE1的活性。陳英偉教授補充說:「這項研究的成功,全賴多學科專業的結合。通過物理學的方法,我們得以觀察ANKLE1如何回應DNA的物理狀態,這是傳統生物學手段難以捕捉的現象。」
基因組穩定性與癌症治療新啟示
該發現大幅推進對細胞在物理張力下維持遺傳物質穩定性的理解。研究揭示ANKLE1作為張力感應型DNA切割酶的角色,為細胞如何防止危險的DNA斷裂、從而避免癌症和其他疾病提供了關鍵線索。
研究亦指出,抑制ANKLE1可能令基因組不穩定的癌細胞進一步失衡,因此抑制ANKLE1可能會讓癌細胞更容易被現有的化療藥物殺死。ANKLE1有望成為癌症治療的新靶點,為利用腫瘤細胞弱點帶來新策略,同時加深對基因組維護機制的理解。