本港癌症新症將於2035年增加四成。
隨着人口老化,香港癌症資料統計中心預測,本港癌症新症將於2035年增加四成。為提升社會對癌症風險評估的認知,近年學界都在積極研究DNA修復系統與癌症之間的關係,而香港大學李嘉誠醫學院的研究團隊最近成功解構一種新型的DNA修復因子「DYRK1B」,有望提供癌症早期病變的檢測方法,為癌症患者提供個人化的治療方案。
點擊看圖輯
港大李嘉誠醫學院研究團隊,成功解構一種新型的DNA修復因子。

香港大學。資料圖片
人體細胞每天都會遭受多達70000項的DNA損傷事件,而DNA修復網絡則負責抵禦這些損傷。若身體的DNA的修復功能異常,或人體過度接觸有害物質,都有機會因修復機制未能趕上復原細胞損傷,而誘發癌症,和高血壓及加促衰老等其他疾病。

港大李嘉誠醫學院研究團隊,成功解構一種新型的DNA修復因子。
港大醫學院的研究團隊最近發現,「DYRK1B」為一種新型的DNA修復因子,這種蛋白激酶被視為代謝綜合症的元兇,其表達的增加,均與癌症病變及化療抗藥性有關。領導是次研究的港大醫學院助理院長及生物醫學學院教授禤承恩表示,有關發現將引導DYRK1B抑製劑的研發和使用,亦會作為與基因組不穩定相關疾病的治療方案。

港大醫學院助理院長及生物醫學學院教授禤承恩。
本港過去近30年的癌症患者不斷上升,過去5年更平均每日有超過35人因癌症離世。禤承恩認為情況和人口老化有莫大關連,由於人體細胞每天都會產生突變和自行修復損傷,人體的基因改變會隨時間不斷累增,故年長人士通常較易患上非遺傳性的癌症。

港大醫學院助理院長及生物醫學學院教授禤承恩。
他續指,研究室的目標為解構DNA受損的反應,及其與患癌的直接關係,成功解構DNA修復機制,不僅能作癌症的風險評估,亦可根據各人基因排序的分別,為患者提供個人化的治療選項,而隨着學界對DNA修復系統的認知加深,他相信會對人類長壽和生活素質有正面影響。
香港大學工程學院研究團隊近日取得一項重要科研突破。他們成功透過機械拉伸技術,令氮化鎵材料的發光顏色實現從「紫外光到藍光」的動態調控。這項技術為未來的先進功率電晶體、光電元件、射頻元件以及微型發光二極管顯示器,提供了全新的半導體材料調控方案。
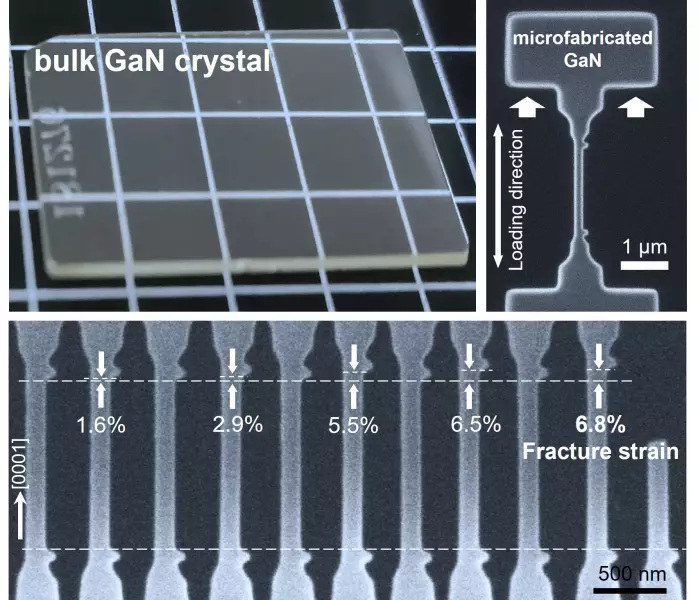
圖示氮化鎵塊體微加工製成單晶微橋。左上為加工前塊體材料;右上為微橋樣品;下圖呈現拉伸測試過程,顯示樣本斷裂前可達6.8%超大彈性應變。港大圖片
實現高達6.8%彈性形變
研究由機械工程系陸洋教授領導,團隊利用微納加工技術,將單晶氮化鎵材料製成微小的橋狀結構。透過精密機械拉伸,使材料產生高達6.8%的彈性形變,其抗拉強度達到約11 GPa。這展現了尺寸效應帶來的非凡彈性變形能力,為深度應變工程開拓了新的發展空間。
圖示氮化鎵塊體微加工製成單晶微橋。左上為加工前塊體材料;右上為微橋樣品;下圖呈現拉伸測試過程,顯示樣本斷裂前可達6.8%超大彈性應變。港大圖片
發光波長從紫外偏移至可見光
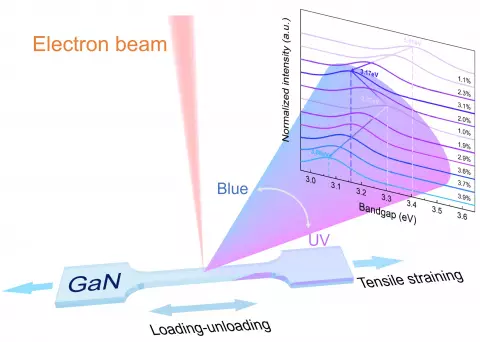
這種物理拉伸不僅沒有損壞材料,反而成功將氮化鎵的發光顏色從原本不可見的紫外光,逐步轉變為肉眼可見的藍色光。在原位力學拉伸結合陰極射線發光系統的實驗中,研究人員實時監測應變過程中的光學特性變化。當拉伸程度達到3.9%時,發光顏色已實現明顯轉變,氮化鎵的帶隙從3.41 eV連續紅移至3.08 eV,發光波長相應從紫外光區進入可見光區。在最大應變條件下,帶隙可進一步降至2.96 eV,波長從約365 nm偏移至420 nm。

應變固定氮化鎵微機械器件應用展示。右上CL光譜測試顯示,當器件鎖定於約3%拉伸應變時,發光帶隙由3.42 eV顯著紅移至3.34 eV。港大圖片
具可逆性與「鎖定」結構設計
氮化鎵是2014年諾貝爾物理學獎藍光LED的核心材料,過去科學家需要透過添加不同化學元素來調節發光顏色。而這次港大的研究展示了一種純物理的調控方法,其獨特之處在於「可逆性」——當撤去拉伸力時,材料會恢復原狀,發光顏色也隨之回到原本的紫外光。這種發光特性隨應變狀態完全可逆的動態調控方式,有別於傳統需要改變材料化學成分的方法。
研究團隊還設計了一種微型機械結構,能夠將拉伸狀態「鎖定」。透過鎖定約3%的拉伸應變,該元件成功實現了發光波長從363nm到371nm的穩定紅移,在不需要持續外力的情況下保持此應變發光狀態,這項設計讓技術更具實際應用價值。未來,這項技術有望應用於微型顯示器、智能照明,甚至生物感測等領域。
這項研究成果已發表於國際頂級物理學期刊《物理評論X》,文章標題為「Deep Elastic Strain Engineering of Free-Standing GaN Microbridge」。
- 核心技術:透過機械拉伸實現氮化鎵材料發光顏色從紫外光到藍光的動態調控。
- 關鍵數據:拉伸產生高達6.8%的彈性形變;抗拉強度約11 GPa;帶隙可從3.41 eV降至2.96 eV。
- 技術特點:調控過程完全可逆;設計了可「鎖定」拉伸狀態的微型機械結構。
- 應用前景:為先進功率電晶體、光電元件、微型LED顯示器、智能照明及生物感測等領域提供新方案。