長江生命科技集團有限公司宣佈成立科學顧問委員會。該委員會乃策略性組織,由來自學術界、臨床研究及業界的獨立專家所組成。科學顧問委員會將提供科學、臨床及規管指引,以支持長江生命科技之科研項目全速前進,包括多項正準備展開臨床研究的治療性癌症疫苗。

圖片來源:長江生命科技2024年度年報
科學顧問委員會將提供專業資源,以助公司應對日趨繁複的環球藥物研發環境、緩減風險,以及加快獲得監管批核和接觸病患者的途徑。
長江生命科技副主席余英才欣見科學顧問委員會之成立,余氏表示:「此舉乃長江生命科技的重要里程碑,標誌著公司進入科學發展的新階段。科學顧問委員會之成員將為公司帶來世界級的專業知識,他們的指導將有助加速我們的創新療法研究進程,並可望革新對病患者的護理。」

長江生命科技委任高永文醫生為科學顧問委員會主席。FB圖片
長江生命科技委任高永文醫生為科學顧問委員會主席。作為香港備受尊敬的公共衞生領袖,高醫生將指引委員會的方向,匯聚專業見解並轉化為有利公司之策略建議。
高永文醫生稱: 「本人很榮幸出任為科學顧問委員會的主席。長江生命科技致力推動科研發展,旗下研發項目別具潛力,可切合現時尚未被滿足的醫療需求。我期望與委員會各成員合作,提供獨立專業意見,促進科研在嚴謹的過程中穩步發展,並支持負責任的創新。」
長江生命科技集團有限公司(「長江生命科技」;港交所代號:0775)宣布,旗下處於發展階段之生物製藥公司 Dogwood Therapeutics, Inc.(「Dogwood」;納斯達克股票代碼:DWTX)公佈正在進行之 Halneuron®第 2b 期因化療引致之神經痛症(chemotherapy-induced neuropathic pain「CINP」)研究之中期分析取得正面結果。

生物製藥公司 Dogwood Therapeutics官網截圖
獨立統計審查委員會審閱 97 名完成治療患者之非盲法治療數據後,所得結論乃於為期四星期之研究中,就改善疼痛方面而言,接受 Halneuron®治療之患者與接受安慰劑治療之患者之間存在正面差異。根據目前第 2b 期試驗之招募速度及中期評估結果,Dogwood 仍預計將在 2026 年第三季內獲得初步結果。目前之研究患者招募趨勢預計將可提供約 80% 至 85% 之統計功效,以檢測 Halneuron® 治療差異。
長江生命科技官網截圖
長江生命科技執行董事兼副主席余英才先生表示:「是次獨立中期分析之結果令人鼓舞,不僅加強我們對 Halneuron®有望成為目前缺乏標準療法之 CINP 患者提供治療選擇之信心,也印證我們透過策略性佈局,以 Dogwood 研發疼痛及相關病症藥物之前瞻視野。」
生物製藥公司 Dogwood Therapeutics官網截圖
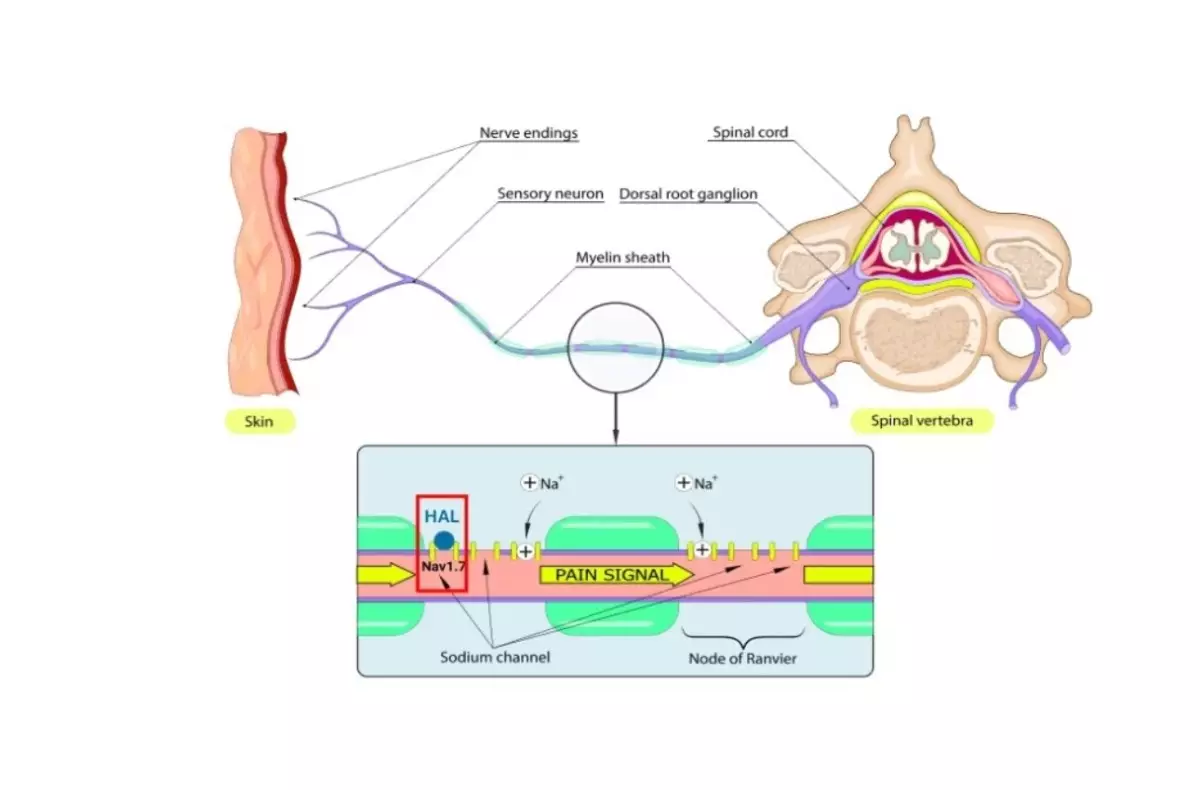
是次 Halneuron®治療效果的初步證據值得關注,基於中期分析群組中患者平均 CINP 患期為5年,且 67%之患者同時接受其他慢性疼痛藥物之穩定劑量治療。此外,該研究的整體退出率約 4.4%,遠低於其他美國食品及藥物管理局 ( U.S. Food and Drug Administration「FDA」)批准之慢性疼痛藥物之退出率。儘管目前仍處於盲法階段,惟 Dogwood 認為是項發現再次證明 Halneuron®在先前臨床試驗中觀察所得令人鼓舞之安全性及耐受性。
Halneuron®乃非鴉片類 Nay 1.7 抑制劑,目前已獲 FDA 授予治療 CINP 之快速通道資格認定(Fast Track designation)。本次第 2b 期研究完成後,結果將為開展第三期確證性臨床試驗奠定基礎,並有助推動與監管機構就註冊路徑達成共識。















