聖地牙哥--(BUSINESS WIRE)--2026年4月7日--
艾卡迪亞製藥公司(Acadia Pharmaceuticals Inc.)(納斯達克:ACAD)今日宣布,DAYBUE® STIX(trofinetide)口服溶液現已在美國廣泛供應,用於治療兩歲及以上成人和兒童雷特綜合症(Rett syndrome)患者。這款新配方是一種不含染料和防腐劑的trofinetide粉末製劑,已於2025年12月獲美國食品及藥物管理局(FDA)批准。其生物等效性與原有的DAYBUE®口服溶液相同,提供相同的療效和安全性。新配方為雷特綜合症患者提供更多彈性,可自行選擇DAYBUE治療的劑量和口味。

艾卡迪亞製藥公司宣布,DAYBUE® STIX(trofinetide)現已在美國廣泛供應,用於治療雷特綜合症。 AP圖片
艾卡迪亞首席商務官湯加納(Tom Garner)指出:「初步回饋顯示,在有限推出後,一小部分護理人員中逾八成早期使用者對DAYBUE STIX表示滿意,這突顯了新配方所帶來的額外彈性和便攜性。我們聽聞新配方或能讓現實環境中的護理更具個性化。持續評估患者和護理人員的意見仍然是我們的首要任務;他們對於我們如何更好地協助管理這種複雜病症的家庭至關重要。」
近期一份關於trofinetide在雷特綜合症實際應用專家建議的刊物,亦強調了靈活、以患者為中心方法的重要性。一個由國際雷特綜合症基金會(IRSF)指定卓越中心(COEs)專家組成的指導小組達成共識,確認trofinetide口服溶液為雷特綜合症患者標準護理的一部分。他們亦就早期開始治療和長期持續使用等關鍵實際考量達成一致。這些建議亦反映了在臨床實踐中需要個性化決策的共同觀點,以助優化患者、家庭和護理人員的治療成果。
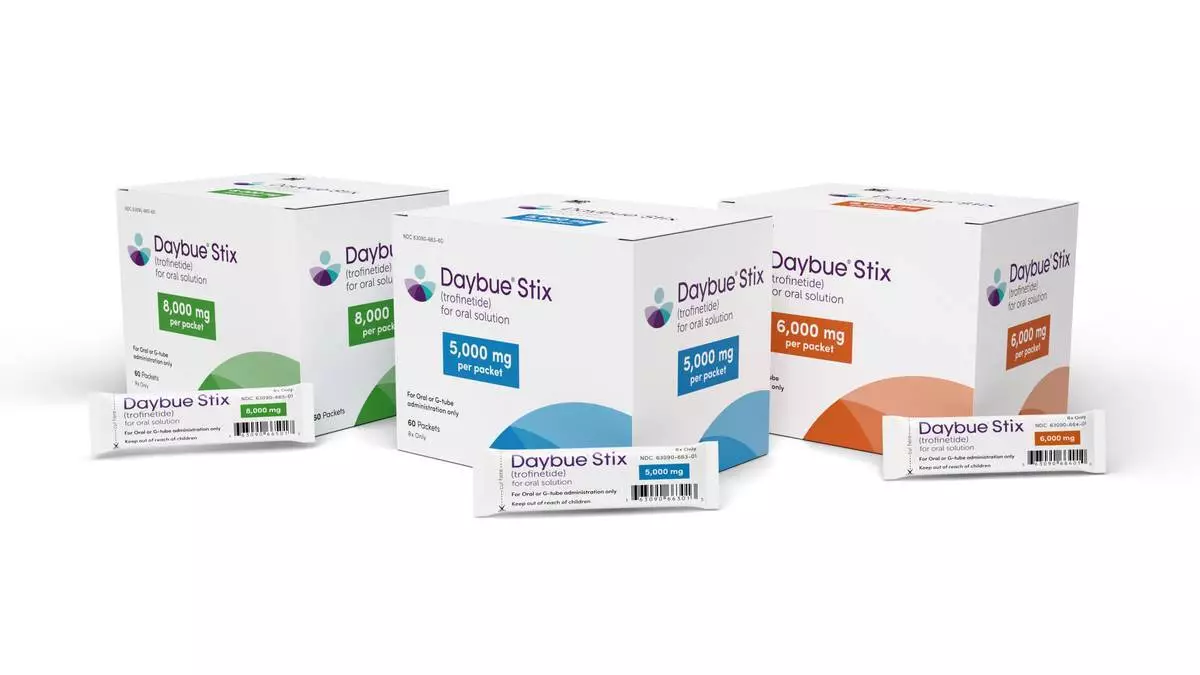
艾卡迪亞製藥公司宣布,DAYBUE® STIX(trofinetide)現已在美國廣泛供應,用於治療雷特綜合症。 AP圖片
明尼蘇達州聖保羅吉列兒童專科醫療中心(Gillette Children's Specialty Healthcare)兒科部亞瑟貝桑醫生(Arthur Beisang, M.D.)表示:「DAYBUE STIX的推出,為我們提供了一種額外且靈活的方式來施用trofinetide,讓我們有更多選擇來滿足獨特的患者和護理人員需求。這種以患者為中心的方法,與近期發布的專家共識建議相符,該建議倡導將trofinetide整合為標準護理和全面雷特綜合症管理的一部分。這個新選項提供了額外的個性化,支持雷特綜合症患者的個別化護理。」
DAYBUE STIX是一種口服溶液粉末,護理人員可將其與各種水性液體混合,例如果汁、茶、檸檬水或液體補充劑,以便護理人員可根據其親人的口味進行定制。該產品以獨立包裝提供,方便攜帶。
DAYBUE STIX的療效和安全性,乃基於DAYBUE口服溶液在雷特綜合症患者中進行的關鍵性三期LAVENDER™研究結果。新配方的批准,則參考了一項生物等效性研究的結果,該研究證明原有的DAYBUE口服溶液和新的DAYBUE STIX口服溶液粉末配方,均提供可比的藥物暴露量。
有興趣探索此新選項的家庭,應諮詢其醫療服務提供者。艾卡迪亞亦為家庭提供Acadia Connect®的支援計劃,該計劃提供一支專業且經驗豐富的支援團隊,在整個DAYBUE治療過程中,為患者和護理人員提供財務資源和處方支援。美國食品及藥物管理局於2023年批准的原有口服溶液配方將繼續供應。
關於雷特綜合症
雷特綜合症是一種罕見、複雜的神經發育障礙,可能分為四個階段,全球每1萬至1.5萬名女嬰中約有一人患病。在美國,約有6,000至9,000名患者受影響。患有雷特綜合症的兒童在6至18個月大之前,會經歷一段看似正常的早期發育期,之後其技能似乎會減慢或停滯。這通常會伴隨一段退化期,期間兒童會失去已習得的溝通能力和有目的的手部使用。兒童隨後可能會經歷一個平台期,其認知興趣會輕微恢復,但身體動作仍嚴重受損。隨著年齡增長,雷特綜合症患者可能會繼續經歷一個運動功能惡化階段,這可能持續患者的餘生。雷特綜合症通常由MECP2基因突變引起。在臨床前研究中,MeCP2功能缺陷被認為會導致突觸通訊受損,而突觸功能缺陷可能與雷特綜合症的表現有關。
雷特綜合症的症狀亦可能包括手部刻板動作,例如搓手和拍手,以及步態異常。大多數雷特綜合症患者通常能活到成年,並需要全天候護理。
關於DAYBUE®(trofinetide)和DAYBUE® STIX(trofinetide)
Trofinetide是胰島素樣生長因子-1 N端三肽的合成類似物。Trofinetide在雷特綜合症患者中發揮治療作用的機制尚不清楚。在動物研究中,trofinetide已被證明能增加樹突的分支和突觸可塑性信號。
DAYBUE®(trofinetide)和DAYBUE® STIX(trofinetide)的適應症和重要安全資訊
適應症
DAYBUE和DAYBUE STIX適用於治療兩歲及以上成人和兒童雷特綜合症患者。
重要安全資訊
DAYBUE以口服溶液(200毫克/毫升)形式提供。
DAYBUE STIX口服溶液粉末以5,000毫克、6,000毫克和8,000毫克包裝提供。
請閱讀完整的處方資訊,亦可於DAYBUEhcp.com查閱。
關於艾卡迪亞製藥公司
艾卡迪亞致力於將科學承諾轉化為有意義的創新,為全球服務不足的神經系統和罕見疾病社群帶來改變。我們的商業產品組合包括首個亦是唯一獲美國食品及藥物管理局批准用於柏金遜症精神病和雷特綜合症的治療方案。我們正透過強大而多元的產品線開發下一波治療進展,其中包括針對阿茲海默症精神病和路易體失智症精神病的處於中期至後期階段的項目,以及解決其他服務不足患者需求的早期項目。在艾卡迪亞,我們旨在為他們帶來改變。欲了解更多資訊,請瀏覽acadia.com並在LinkedIn和X上關注我們。
前瞻性聲明
本新聞稿包含《1995年私人證券訴訟改革法案》所界定的前瞻性聲明。前瞻性聲明包括所有非歷史事實的聲明,並可透過「可能」、「將會」、「應該」、「預期」、「預計」等詞語及類似表達(包括其否定形式)來識別,旨在識別前瞻性聲明。本新聞稿中包含的前瞻性聲明包括但不限於以下內容:(i) DAYBUE和DAYBUE STIX的療效和安全性,以及預期的雷特綜合症症狀改善,(ii) DAYBUE STIX在給藥方面的靈活性和允許個性化護理,(iii) 將DAYBUE和DAYBUE STIX用作雷特綜合症患者的標準護理,以及 (iv) DAYBUE和DAYBUE STIX的潛在未來用途。前瞻性聲明受已知和未知風險、不確定性、假設及其他因素的影響,這些因素可能導致我們的實際結果、表現或成就與我們的前瞻性聲明所預期或暗示的內容存在重大差異。此類風險、不確定性、假設及其他因素包括但不限於:我們能否繼續成功將DAYBUE和DAYBUE STIX商業化,以及我們能否繼續遵守適用法律和法規。鑑於這些風險和不確定性,您不應過度依賴這些前瞻性聲明。有關這些及其他可能導致我們的實際結果、表現或成就出現差異的風險、不確定性、假設及其他因素的討論,請參閱我們於2026年2月26日向證券交易委員會提交的截至2025年12月31日止年度的10-K表格年度報告,以及我們不時向證券交易委員會提交的後續文件。本文所載的前瞻性聲明乃截至本文發布之日作出,除法律要求外,我們不承擔在此日期之後更新這些聲明的義務。
(美聯社)