健康管理與抗衰中心Humansa宣佈,與由莫仲棠教授創辦的香港中文大學衍生企業思瞳科研合作,推出創新的Humansa BrainSpark腦部健康計劃。該計劃採用全球首個人工智能(AI)模型,僅透過視網膜影像即可檢測阿茲海默症風險,為腦部健康管理帶來非侵入性且易於獲取的解決方案,應對亞太地區日益嚴峻的認知衰退挑戰。

Humansa BrainSpark腦部健康計劃專為亞太地區健康挑戰設計。當地平均壽命已達85歲,但85歲及以上長者中每三人就有一人可能罹患認知障礙,此疾病會逐漸侵蝕患者獨立生活能力與生命品質。「研究顯示,優化可調節風險因素可預防或延緩45%認知障礙病例,因此早期檢測與個性化干預至關重要。」計劃強調。

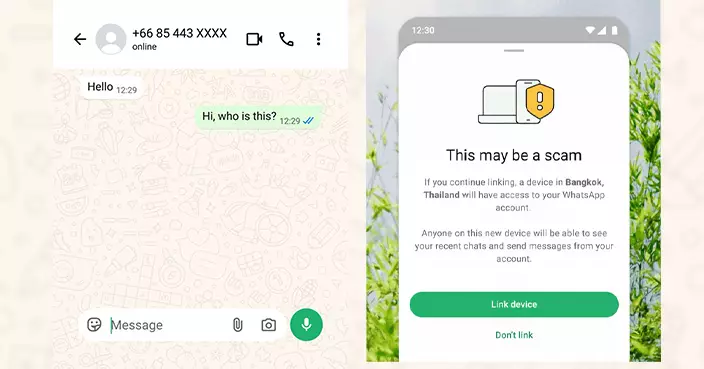
Humansa 指亞太地區85歲及以上長者中每三人就有一人可能罹患認知障礙。巴士的報記者攝
該計劃以積極態度維護大腦健康,提供全面腦健康評估與個性化生活方式干預方案。核心技術為中大莫慶堯醫學教授莫仲棠教授團隊研發的AI視網膜影像技術(i-Cog Brain Health),透過分析648名阿茲海默症患者與3,240名認知正常者的近1.3萬張視網膜影像,經開發與驗證雙重階段,於多種族、多國家數據中達80%至92%準確率。研究由香港中文大學領導,聯合新加坡國立大學、清華大學、梅奧診所及貝爾法斯特女王大學合作完成,成果於202年發表於《刺針數字健康》期刊。
「視網膜是大腦延伸,其非侵入性攝影可捕捉阿茲海默症相關早期血管與神經病變——這些變化早於臨床症狀10-15年,為干預創造黃金窗口。」i-Cognitio Sciences創始總監、中大莫慶堯醫學教授莫仲棠教授解釋,「我們的AI模型能識別傳統MRI難以檢測的微血管異常,成為臨床及社區篩查高危人群的革命性工具。」
莫教授進一步強調:「計劃整合前沿AI技術與Humansa個性化抗衰方案,實現雙軌突破——推動早期預防性治療與促進生活方式干預。此主動式腦健康管理能有效延緩認知衰退,提升長期生活品質。」

Humansa管理團隊與嘉賓在Humansa BrainSpark 腦部健康計劃活動上合影 (左起:Humansa 國際諮詢委員會成員Dr. Sanja Tomovska, Humansa 創始合夥人江琳,中大莫慶堯醫學教授莫仲棠教授,Humansa首席商業與應用人工智慧官王智超,Humansa健康管理導師蘇芷雯,Humansa 行政總裁蘇嘉威
作為Humansa抗衰戰略延伸,新計劃是其標誌性「Future Health健康計劃」核心組成,體現「預防優先、早期檢測、個性化策略」的抗衰理念。Humansa首席執行官蘇嘉威(Don So)表示:「我們相信衰老是可掌握的技能、主動的選擇,更是精密科學。認知功能是抗衰戰略關鍵支柱,直接決定獨立生活能力與生活品質。症狀未顯現時,健康風險種子已悄然播下。BrainSpark計劃透過先進科學工具,賦能大眾延長健康週期,活出更長久、優質的人生。」Humansa BrainSpark腦部健康計劃的突破性在於整合AI技術與個性化健康管理,為認知防護開闢新路徑,重新定義腦健康維護方式,為追求長壽與高品質生活者提供實操方案。