BOSTON--(BUSINESS WIRE)--Apr 2, 2026--
Seaport Therapeutics(下稱「Seaport」或「公司」)是一家臨床階段治療公司,致力於推進新型神經精神藥物。公司今日公布其第一期概念驗證臨床試驗GlyphAgo™ (SPT-320™ 或 Glyph Agomelatine) 的初步結果。該試驗評估一種新型、Glyphed口服阿戈美拉汀(agomelatine)前體藥物,旨在治療廣泛性焦慮症(generalized anxiety disorder, GAD)。初步結果顯示,GlyphAgo的生物利用度較未經修飾的阿戈美拉汀增加逾兩倍,達到治療水平。同時,它顯著降低肝臟暴露,預計可減少或免除肝功能測試的需要。
Seaport Therapeutics公布GlyphAgo一期試驗初步結果 廣泛性焦慮症新藥潛力大 AP圖片
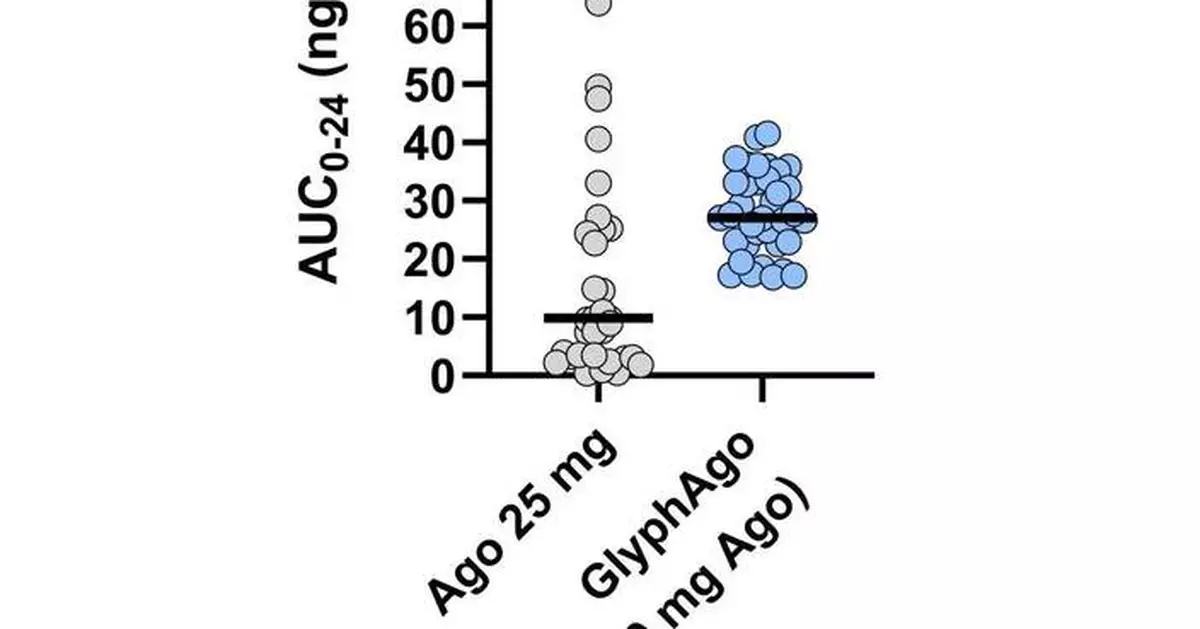
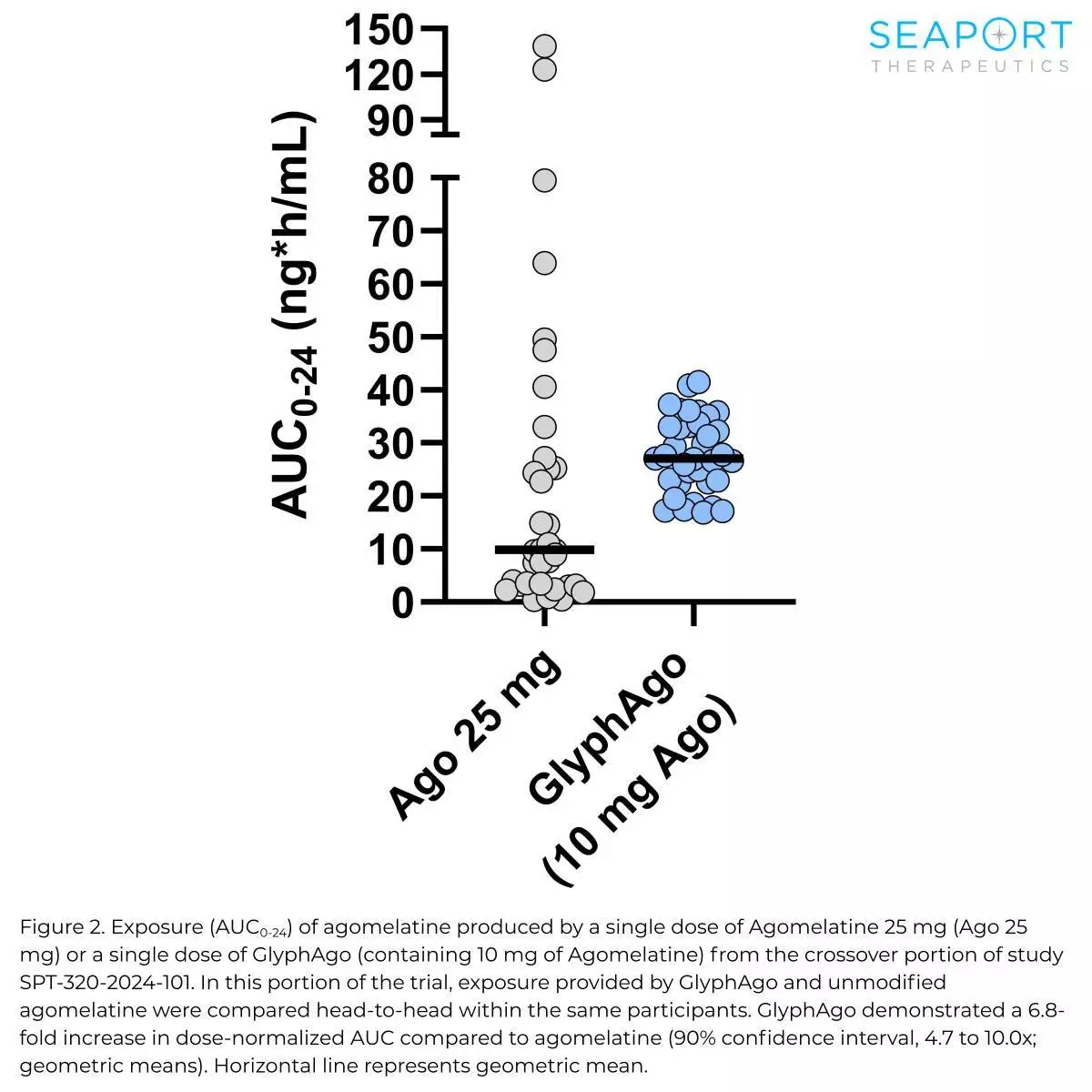
在試驗的頭對頭交叉部分,GlyphAgo的阿戈美拉汀生物利用度較未經修飾的口服阿戈美拉汀增加6.8倍。GlyphAgo的藥代動力學變異性亦顯著降低(10倍),優於未經修飾的阿戈美拉汀。交叉試驗部分包括服用含雌激素口服避孕藥(estrogen-containing oral contraceptives)的參與者,已知這些藥物會因肝臟藥物相互作用而增加阿戈美拉汀的暴露。相反,GlyphAgo的暴露不受口服避孕藥影響,進一步支持GlyphAgo能繞過肝臟首關代謝。在試驗的另一單次遞增劑量部分,GlyphAgo的劑量標準化暴露較阿戈美拉汀增加9.6至14.5倍,該部分參與者並無服用口服避孕藥。GlyphAgo耐受性良好,未觀察到任何肝臟相關不良事件。已完成的單次遞增劑量及交叉試驗部分共涉及約130名參與者,達成了試驗的藥代動力學概念驗證目標。目前進行中的多次遞增劑量部分(僅使用GlyphAgo)旨在進一步闡明GlyphAgo重複給藥的安全性及藥代動力學。
Seaport Therapeutics聯合創辦人兼行政總裁Daphne Zohar指出:「這些來自充分設計的第一期試驗的初步數據,加強了我們對GlyphAgo潛力的信心,並為Glyph平台提供了進一步的臨床驗證。」她續稱:「基於這些數據,我們計劃將GlyphAgo推進至兩項平行試驗:一項第二期a藥理學概念驗證試驗,旨在評估GlyphAgo對廣泛性焦慮症患者潛在的睡眠益處;以及一項第二期b試驗,這是一項隨機安慰劑對照試驗,旨在具備註冊潛力。我們相信GlyphAgo有潛力為廣泛性焦慮症患者帶來數十年來美國首個針對這種未獲充分服務且具致殘性的疾病的新療法。」
Seaport Therapeutics公布GlyphAgo一期試驗初步結果 廣泛性焦慮症新藥潛力大 AP圖片
阿戈美拉汀是一種經臨床驗證的MT1/MT2褪黑激素受體激動劑及血清素2C (5-HT2C)受體拮抗劑,是一種有效的抗焦慮藥及抗抑鬱藥,已獲澳洲及歐盟批准用於治療廣泛性焦慮症,並獲澳洲及歐盟批准用於治療重度抑鬱症(major depressive disorder, MDD)。阿戈美拉汀在澳洲及歐盟的標籤均要求在開始治療前、治療期間及增加劑量時進行肝功能測試。阿戈美拉汀尚未獲美國批准。
Seaport Therapeutics聯合創辦人兼董事會主席Steven Paul醫生表示:「在廣泛性焦慮症方面,阿戈美拉汀在四項第三方安慰劑對照研究中,已顯示出與安慰劑之間穩健且具統計學意義的差異,並在薈萃分析中觀察到其療效及耐受性優於選擇性血清素再攝取抑制劑(selective serotonin-reuptake inhibitors)或苯二氮卓類藥物(benzodiazepines)。」他續指:「儘管具有這種積極的特性,逾九成未經修飾的阿戈美拉汀在首關代謝中流失,其使用亦因劑量依賴性肝酶升高而受到限制。GlyphAgo增強的藥物特性及其導致的阿戈美拉汀全身暴露個體間變異性顯著降低,支持我們在廣泛性焦慮症中對GlyphAgo的臨床開發。」
利用Seaport的專有Glyph™平台,GlyphAgo旨在增強淋巴吸收並避免肝臟首關代謝,從而提高口服生物利用度並減少副作用。透過利用膳食脂肪所使用的腸道淋巴系統作為替代吸收途徑,GlyphAgo旨在增加阿戈美拉汀的全身暴露,使其在廣泛性焦慮症中達到有效暴露水平,但劑量較低,從而減少肝臟暴露並減少或免除肝功能測試的需要。根據Seaport迄今為止產生的數據,GlyphAgo有潛力成為廣泛性焦慮症的主要治療方法。
Seaport Therapeutics聯合創辦人兼平台高級副總裁Daniel Bonner博士指出:「阿戈美拉汀結合了獨特的機制與在廣泛性焦慮症中良好的療效及耐受性,但其潛力此前因肝臟首關代謝及繁瑣的肝功能測試需求而受到限制。」他續稱:「這些結果顯示GlyphAgo超越了生物利用度的目標改善,實現了穩健的暴露,並在顯著較低的阿戈美拉汀劑量下呈現出更一致的藥代動力學特性。」
第一期試驗設計
該第一期概念驗證試驗分多個部分進行,旨在評估GlyphAgo的安全性、耐受性及藥代動力學,並將GlyphAgo的藥代動力學與單獨使用阿戈美拉汀進行比較。試驗包括單次及多次遞增劑量組,以及交叉試驗部分(包括食物效應及參與者內部GlyphAgo與阿戈美拉汀的比較),採用開放標籤及安慰劑對照設計。在第一期試驗的單次遞增劑量部分,健康志願者單次服用遞增劑量的GlyphAgo或25毫克劑量的阿戈美拉汀(澳洲及歐盟批准的有效劑量),以評估藥代動力學參數,包括藥時曲線下面積(Area under the curve, AUC,衡量總暴露量)及血漿峰濃度(Cmax)。在單次遞增劑量部分,參與者為無肝功能損害證據的健康志願者,並未服用任何已知會改變阿戈美拉汀藥代動力學的藥物或補充劑,包括氟伏沙明(fluvoxamine)或含雌激素口服避孕藥。在交叉試驗部分,參與者被隨機分配到兩個序列之一,旨在評估食物對單一劑量GlyphAgo的影響,並將其與25毫克劑量的阿戈美拉汀進行比較。兩個序列均在阿戈美拉汀之前評估GlyphAgo在進食及空腹狀態下的情況,這種結構旨在避免將GlyphAgo的安全性結果與阿戈美拉汀已知的肝毒性混淆。
初步結果
交叉試驗部分
- GlyphAgo的阿戈美拉汀生物利用度較未經修飾的口服阿戈美拉汀增加6.8倍。
- GlyphAgo的藥代動力學變異性較未經修飾的阿戈美拉汀顯著降低10倍。
- GlyphAgo的暴露不受含雌激素口服避孕藥影響。
單次遞增劑量部分
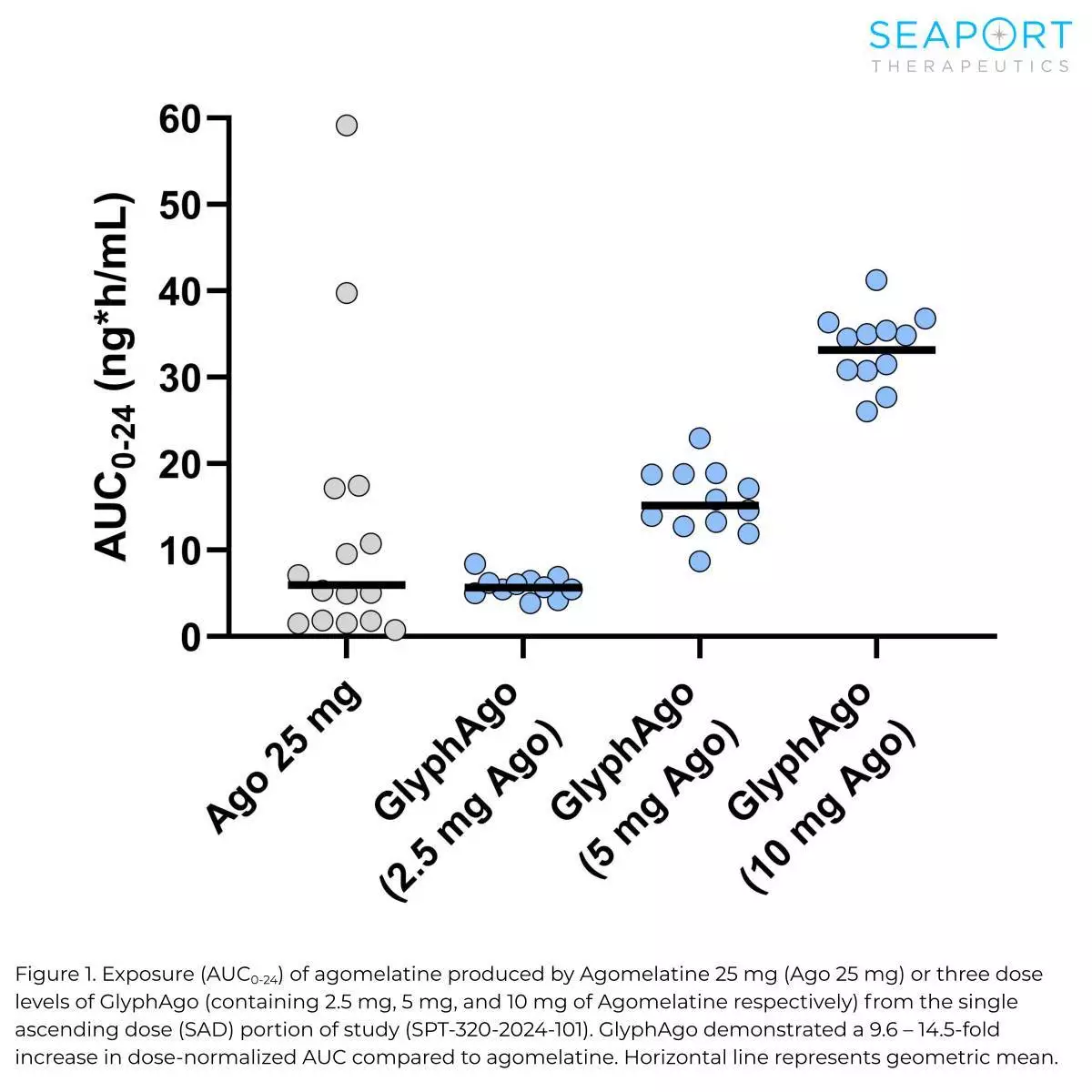
- GlyphAgo的劑量標準化暴露較阿戈美拉汀增加9.6至14.5倍。
- GlyphAgo耐受性良好,未觀察到肝臟相關不良事件。
Seaport計劃在未來即將舉行的科學會議上,公布第一期試驗的額外分析,包括多次遞增劑量部分的結果。
關於GlyphAgo (SPT-320 或 Glyph Agomelatine)
GlyphAgo是一種新型、Glyphed口服阿戈美拉汀前體藥物,阿戈美拉汀是一種經臨床驗證的抗焦慮藥及抗抑鬱藥,已獲澳洲及歐盟批准用於治療廣泛性焦慮症,並獲澳洲及歐盟批准用於治療重度抑鬱症。利用Seaport的專有Glyph平台,GlyphAgo旨在避免肝臟首關代謝並增加阿戈美拉汀的全身暴露,使其在廣泛性焦慮症中達到有效暴露水平,但劑量較低,從而減少肝臟暴露並減少或免除肝功能測試的需要。根據內部分析,Seaport相信GlyphAgo給藥可將阿戈美拉汀的生物利用度提高兩倍,從而減少或消除肝酶升高。根據迄今為止產生的數據,Seaport相信GlyphAgo有潛力成為廣泛性焦樂症的主要治療方法。
關於Seaport Therapeutics
Seaport Therapeutics是一家臨床階段治療公司,致力於在未獲滿足患者需求高的領域推進新型神經精神藥物的開發。公司擁有一項經證實的策略,即推進此前因其專有Glyph技術平台的局限性而受阻的臨床驗證機制。其一流及同類最佳藥物管線中的所有治療候選藥物均基於Glyph平台,該平台獨特設計旨在實現口服生物利用度、繞過首關代謝並減少肝酶升高或肝毒性及其他副作用。Seaport由一支經驗豐富的團隊領導,該團隊曾發明並推進重要的神經精神藥物,並由廣泛的知名科學家、臨床醫生及主要意見領袖網絡提供指導。
(美聯社)