沙田區一所中學爆發肺癆個案,共七名學生及一名職員感染。衞生署指九月初接獲呈報沙田一所中學學生感染結核病,全部病人現時情況穩定,學校正常上課。翻查沙田區學校資料,發現沙田蘇浙公學在今年九月發出通告,稱該校一名中四級學生確診肺結核桿菌感染,衞生署建議接觸緊密的老師及同學接受胸部X光檢驗。有醫生指,香港約兩成人為肺結核帶菌者,但一般中學生非高危人士,認為事件屬罕見。

衛生署證實,沙田有中學爆發肺癆(資料圖片)
結核病由結核桿菌所引起,主要感染肺部形成肺結核病,俗稱肺癆,分為較高傳染性的開放式肺癆,以及非開放式肺癆,肺結核病人咳嗽或打噴嚏時會將細菌散播到空氣中,抵抗力稍差的人吸入後便會染病。
點擊看圖輯
肺癆分為較高傳染性的開放式肺癆,以及非開放式肺癆(資料圖片)
沙田蘇浙公學今年九月發出通告,指該校一名中四級學生確診肺結核桿菌感染(資料圖片)
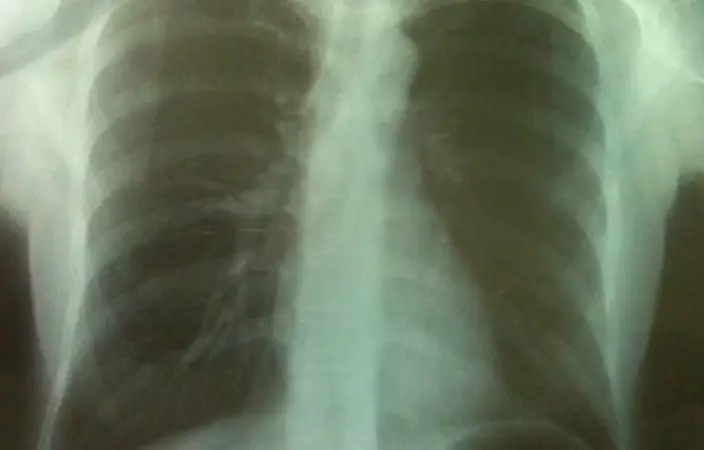
肺癆分為較高傳染性的開放式肺癆,以及非開放式肺癆(資料圖片)
衛生署證實,署方胸肺科九月初接獲呈報沙田一所中學學生的結核病個案,並即時聯絡該校跟進,經調查後發現七名學生及一名職員受感染,全部病人現時情況穩定,學校正常上課,已安排校內接觸比較緊密的師生接受潛伏性結核病篩查,有需要時會給予預防性治療,並已在該校舉行有關結核病的健康講座。
翻查沙田區學校資料,發現沙田蘇浙公學在今年九月二十八日向全校中一至中六學生發出通告,標題為「預防肺結核傳播,胸部X光檢驗」,稱收到衞生署胸肺科診所通報該校一名中四級學生確診受到肺結核桿菌感染,現正接受治療,在家休息。由於此桿菌有一定的傳染風險和潛伏期,衞生署建議與該名學生接觸緊密的老師及同學須接受胸部X光檢驗。

沙田蘇浙公學今年九月發出通告,指該校一名中四級學生確診肺結核桿菌感染(資料圖片)
通告指校方已和衞生署轄下之粉嶺X光診斷中心聯絡,並安排於十月九日上午為學生免費檢查。並請家長密切留意學生之身體狀況,若有出現持續咳嗽、痰中帶血、體重驟降或午後發燒等病徵,必須盡快求診並通知學校。
香港大學榮譽臨牀肋理教授黃敬恩認為事件罕見,表示肺癆多出現在長者、腎病病人、愛滋病病人等,一般中學生並非高危人士。他指,肺癆病徵「是十分沒有具體性,比較常見是咳血、午夜倒汗,晚上睡覺一身汗,一身汗是指底衫濕透,當然亦會發燒,可以是高燒,溫度會大上大落,咳嗽會長逾三星期,體重下降及食欲不振」。

黃敬恩認為事件罕見(資料圖片)
黃又指,香港兩成人為肺結核帶菌者,肺癆九成個案非直接傳播,「多數是以前被傳染,潛伏在個人體內,例如飲酒或多病,免疾力差才會病發,潛伏期是可以很長」,因此難以追查感染源頭。他估計衛生署會先從患者長時間緊密接觸的人身上作出篩查,例如家人、同班同學或師生等,由於病人已沒有上課,認為現時沒有停課必要。
根據衛生防護中心資料,香港上年共有約四千四百宗結核病呈報數字,即每十萬人約六十人感染,當中死亡個案達一百五十五人,每十萬人約兩人死亡。衛生署指,結核病仍是本港常見傳染病,不時會有一些個案在學校中出現。病者通常在求診時被發現,由醫生呈報,衞生署胸肺科會按需要通知學校。
現時香港特區是按《藥物臨牀試驗質量管理規範》(Good Clinical Practice, 簡稱 GCP)的要求審批藥品的臨牀試驗申請,獲國際認可。此外,香港特區亦有四所臨牀試驗機構共31項專業獲得國家藥品監督管理局的認證 。

為進一步做好超級聯繫人的角色,香港特區正積極籌備申請成為國際人用藥品註冊技術協調會(International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use,簡稱ICH)的監管機構成員,讓本港藥品註冊技術標準對接國際,提升香港在藥品監管領域的競爭力和國際影響力,並推動年底成立的「香港藥物及醫療器械監督管理中心」長遠發展成為藥械領域的國際權威機構。

ICH E6 GCP是香港申請成爲 ICH 監管機構成員前,必須落實的的核心要求之一。作為ICH的「一級指導原則」之一,ICH E6 GCP涵蓋臨床試驗的倫理原則及數據的質量與完整性,確保試驗參與者的權益與試驗數據的科學可靠性,是全球醫藥研發領域共同遵循的嚴謹國際標準。
認識臨牀試驗
新藥研發是一項循序漸進的科學驗證過程,任何新藥從實驗室研發到成功註冊並作廣泛應用,必須經過臨床試驗階段。在香港,進行以人作爲試驗參與者的藥劑製品臨牀試驗前,相關機構必須先向衞生署申請臨牀試驗證明書 (https://www.drugoffice.gov.hk/eps/do/tc/pharmaceutical_trade/guidelines_forms/useful_guidelines_forms.html )。
臨牀試驗一般分為四個階段,各階段均有明確的科學目的,以驗證藥物的有效性和安全性。
· 第一期:通常招募20至80名健康志願者,主要評估藥物的安全性和耐受性。
· 第二期:通常招募數十至數百名志願者,探索藥物的初步療效,進一步確認其安全性,並為第三期試驗確定合適劑量與方案。
· 第三期:通常招募數百至數千名受試者,一般為大規模、隨機、對照的關鍵性試驗,透過與現有標準療法或安慰劑作比較,確認藥物的臨牀效益,同時收集的安全性資料有助識別較罕見的不良反應。
· 第四期: 藥物獲批上市後的後續應用研究,旨在考察藥物在廣泛使用後的療效和不良反應,評估在不同人群中的長期安全性。
ICH E6《藥物臨牀試驗質量管理規範》概要與試驗參與者權益
開展臨床試驗前,科研人員對受試藥物(尤其是創新藥品)的認識多來自動物實驗數據,因此遵循嚴格的國際標準以保障試驗參與者的權益、安全和福祉至關重要。ICH E6 GCP涵蓋整個臨牀試驗過程,包括設計、執行、啟動、記錄、監督、評估、分析和報告等環節,確保試驗符合倫理要求,且數據與結果真實可靠。透過統一標準,亦有助促進ICH成員之間對臨床試驗數據的相互認可。
為保障參與者權益,ICH E6 GCP設立多重保護機制:
· 知情同意: 指試驗參與者或其照顧者獲悉臨牀試驗所有相關資訊,並經過充分討論後,確認自願參加臨牀試驗的程序。研究者必須向參與者清楚說明試驗性質、預期受益、潛在風險及替代治療方案。參與者有權隨時無條件退出試驗而不影響其醫療權益。
· 倫理委員會審查:任何臨牀試驗啟動前,必須獲得倫理委員會的批准。委員會是由具醫學及非醫學背景人士組成的獨立機構,負責審查試驗方案、產品基本資料、研究者資歷,以及知情同意的相關資料及程序,確保參與者的權益、安全與福祉得到保障。
· 安全性監測:研究團隊須持續監測並適時向衞生署報告藥物不良反應,以保障參與者的安全。嚴重及非預期的不良反應須盡早呈報,其餘不良反應則應在試驗結束時作總報告。
「香港藥物及醫療器械監督管理中心」將於今年內成立。制度提升後,監管框架將全面與包括ICH在内的國際最佳作業方式接軌。目前,所有獲批的臨牀試驗證明書的臨牀試驗均須符合GCP 原則。未來,隨着ICH E6 GCP指導原則及相關措施全面落實,將進一步保障試驗參與者的權益、安全與福祉,以及所收集數據的質量與完整性,有助香港建立更安全有效的臨床試驗環境,吸引更多中國內地及海外藥企來港進行臨床試驗,帶動本地生物醫藥產業發展,進一步鞏固香港作為國際醫療創新樞紐的橋頭堡地位。