香港大學醫學院與上海復旦大學基礎醫學院的研究團隊合作研發「靜脈注射加光照觸發眼部釋藥」策略,成功將藥物結集於眼部視網膜母細胞瘤,為治療眼部腫瘤提供有效的非侵入性藥物遞送途徑。今次是團隊首次將光響應釋藥的納米藥物用於治療眼部疾病,具有廣泛應用前景。
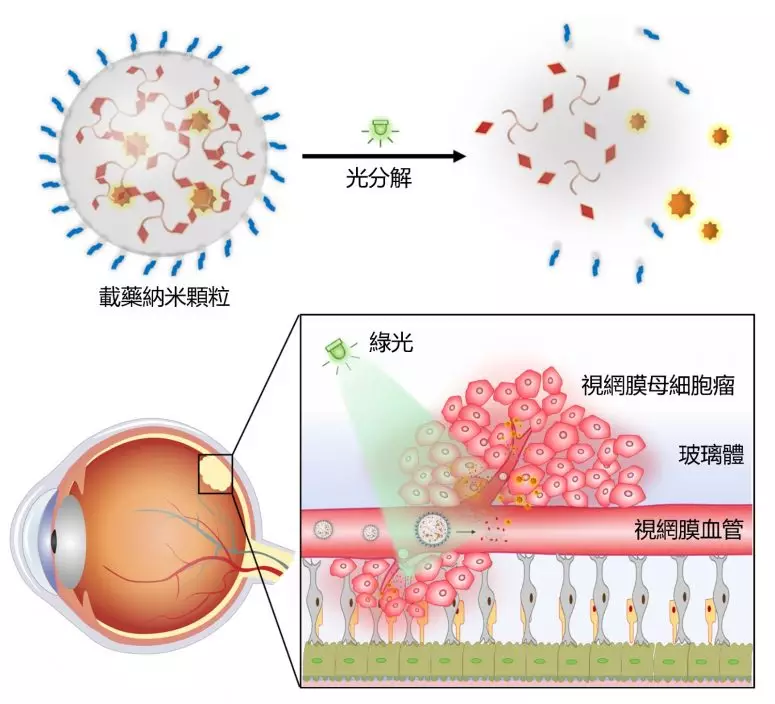
研究團隊設計可被光分解的三枝狀小分子。港大圖片
研究團隊發現,靜脈注射光響應納米藥物後,用光照觸發眼內藥物釋放,可以使藥物在眼內結集並抑制腫瘤的生長。該策略主要基於疏水性藥物在視網膜血管中釋放後,能夠滲入腫瘤組織的特性,克服納米載體於藥物遞送過程中所遭遇的血液—視網膜屏障。
點擊看圖輯
港大醫學院藉光照觸發釋藥系統,取得視網膜母細胞瘤治療新突破。港大圖片

港大醫學院藉光照觸發釋藥系統,取得視網膜母細胞瘤治療新突破。港大圖片
研究團隊設計簡單且可被光分解的三枝狀小分子,該分子可以與疏水性藥物在水溶液中自發組裝形成納米顆粒,並能在綠光照射下分解及釋放藥物。在患有原位視網膜母細胞瘤的小鼠身上,透過靜脈注射納米顆粒並以綠光照射其眼部,可以有效抑制腫瘤生長,且未見毒副作用。

資料圖片
是項研究通過光照觸發釋藥系統,使透過靜脈注射的藥物能在視網膜母細胞瘤中結集,為該腫瘤的治療提供了安全有效的新方法。這項新技術也有助進一步發展精準藥物遞送,以便日後用於治療其他眼部疾病。 有關研究成果已在期刊《先進科學》(Advanced Science)發表,並已申請專利合作條約(PCT)專利。

香港大學。資料圖片
香港大學工程學院研究團隊近日取得一項重要科研突破。他們成功透過機械拉伸技術,令氮化鎵材料的發光顏色實現從「紫外光到藍光」的動態調控。這項技術為未來的先進功率電晶體、光電元件、射頻元件以及微型發光二極管顯示器,提供了全新的半導體材料調控方案。
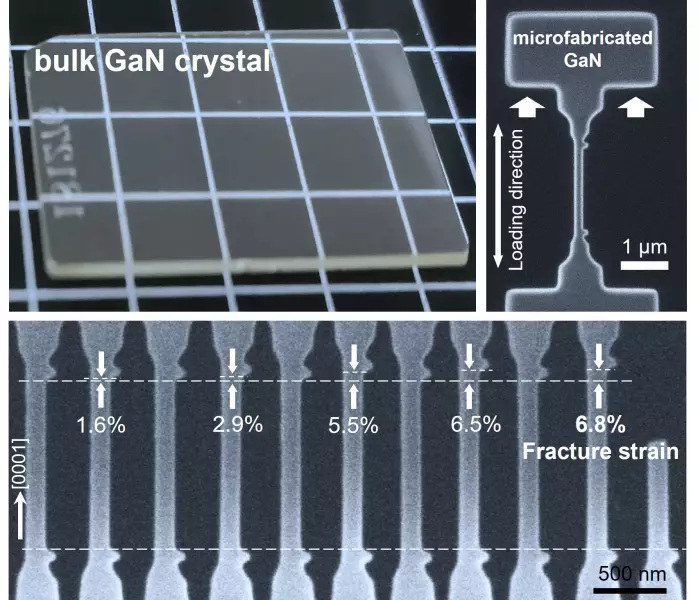
圖示氮化鎵塊體微加工製成單晶微橋。左上為加工前塊體材料;右上為微橋樣品;下圖呈現拉伸測試過程,顯示樣本斷裂前可達6.8%超大彈性應變。港大圖片
實現高達6.8%彈性形變
研究由機械工程系陸洋教授領導,團隊利用微納加工技術,將單晶氮化鎵材料製成微小的橋狀結構。透過精密機械拉伸,使材料產生高達6.8%的彈性形變,其抗拉強度達到約11 GPa。這展現了尺寸效應帶來的非凡彈性變形能力,為深度應變工程開拓了新的發展空間。
圖示氮化鎵塊體微加工製成單晶微橋。左上為加工前塊體材料;右上為微橋樣品;下圖呈現拉伸測試過程,顯示樣本斷裂前可達6.8%超大彈性應變。港大圖片
發光波長從紫外偏移至可見光
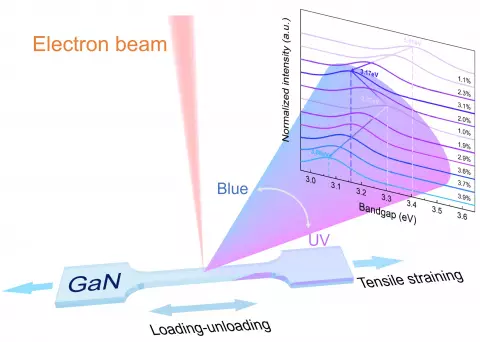
這種物理拉伸不僅沒有損壞材料,反而成功將氮化鎵的發光顏色從原本不可見的紫外光,逐步轉變為肉眼可見的藍色光。在原位力學拉伸結合陰極射線發光系統的實驗中,研究人員實時監測應變過程中的光學特性變化。當拉伸程度達到3.9%時,發光顏色已實現明顯轉變,氮化鎵的帶隙從3.41 eV連續紅移至3.08 eV,發光波長相應從紫外光區進入可見光區。在最大應變條件下,帶隙可進一步降至2.96 eV,波長從約365 nm偏移至420 nm。

應變固定氮化鎵微機械器件應用展示。右上CL光譜測試顯示,當器件鎖定於約3%拉伸應變時,發光帶隙由3.42 eV顯著紅移至3.34 eV。港大圖片
具可逆性與「鎖定」結構設計
氮化鎵是2014年諾貝爾物理學獎藍光LED的核心材料,過去科學家需要透過添加不同化學元素來調節發光顏色。而這次港大的研究展示了一種純物理的調控方法,其獨特之處在於「可逆性」——當撤去拉伸力時,材料會恢復原狀,發光顏色也隨之回到原本的紫外光。這種發光特性隨應變狀態完全可逆的動態調控方式,有別於傳統需要改變材料化學成分的方法。
研究團隊還設計了一種微型機械結構,能夠將拉伸狀態「鎖定」。透過鎖定約3%的拉伸應變,該元件成功實現了發光波長從363nm到371nm的穩定紅移,在不需要持續外力的情況下保持此應變發光狀態,這項設計讓技術更具實際應用價值。未來,這項技術有望應用於微型顯示器、智能照明,甚至生物感測等領域。
這項研究成果已發表於國際頂級物理學期刊《物理評論X》,文章標題為「Deep Elastic Strain Engineering of Free-Standing GaN Microbridge」。
- 核心技術:透過機械拉伸實現氮化鎵材料發光顏色從紫外光到藍光的動態調控。
- 關鍵數據:拉伸產生高達6.8%的彈性形變;抗拉強度約11 GPa;帶隙可從3.41 eV降至2.96 eV。
- 技術特點:調控過程完全可逆;設計了可「鎖定」拉伸狀態的微型機械結構。
- 應用前景:為先進功率電晶體、光電元件、微型LED顯示器、智能照明及生物感測等領域提供新方案。