衞生署的「社區牙科支援計劃」星期一(5月26日)正式推出,增加為有經濟困難的弱勢社群提供獲政府資助的牙科服務,預計可提供現時政府牙科診所牙科街症服務的最少兩倍名額,即每年約4萬人次,現時有32間非政府組織參與計劃,提供近80個牙科服務點,覆蓋全港18區。

社區牙科支援計劃
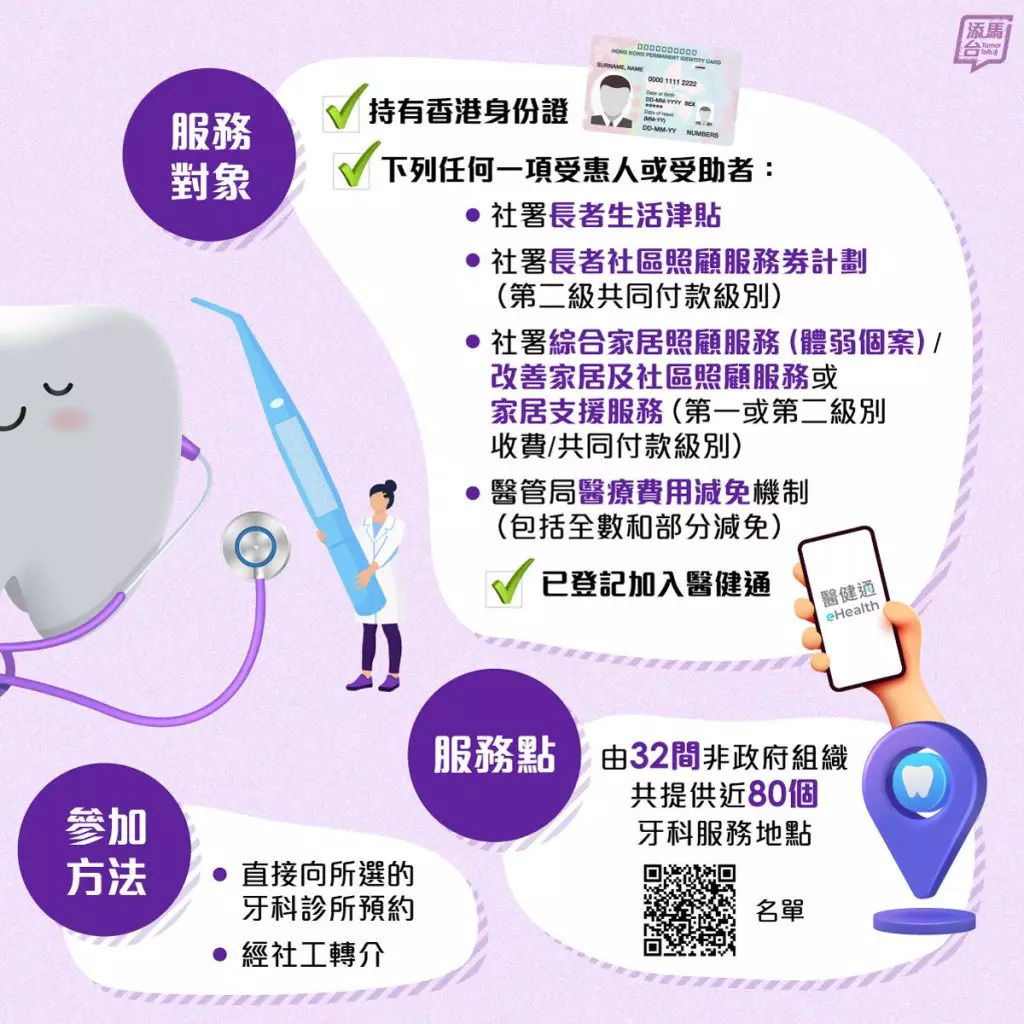
衞生署表示,參加計劃的人士必須持有香港身份證、已登記加入醫健通,以及屬於社署轄下長者生活津貼、長者社區照顧服務券計劃或綜合家居照顧服務的受助人,或獲得減免醫療服務收費資格的醫管局病人。

社區牙科支援計劃
每名參加者每180天可在計劃下申請接受資助牙科服務一次,如果主診註冊牙醫評估後認為情況合適,參加者可獲得口腔檢查、緩解牙齒疼痛的藥物、 X光檢查和補牙或拔牙等指定服務。
發言人表示,每名參加者可以就治理每顆牙齒向非政府組織直接繳付50元行政費,最多繳付150元。合資格人士可獲全數資助行政費。社署轄下綜援計劃的受助人亦可利用牙科治療費用津貼,獲取全面的牙科服務。
社區牙科支援計劃
發言人又說,參加者可透過醫健通流動應用程式,查閱有關就診紀錄,包括就診日期及治療項目,今年稍後亦可透過應用程式查閱相關的電子口腔健康紀錄,以便更清晰了解及監察自己的牙齒狀況。
每一盒藥劑製品出廠前,都必定要經過嚴謹的質量管理系統,符合預設的質量及法規要求才可放行銷售。大家有沒有想過,藥品包裝上的「使用期限」是怎樣設定的?藥品的質量又會如何隨時間變化?
要回答這些問題,關鍵在於藥品的「穩定性」(Stability)。原料藥和成品在生產、運輸、儲存及使用期間,可能會因爲溫度、濕度、光照等環境因素,隨時間發生化學、物理、生物和微生物的變化,導致有效成分降解或產生雜質,影響效能與安全。藥廠會根據藥物成分的特性及配方的前期研究,設計穩定性測試,以科學方法制定藥劑製品標籤上的使用期限。目的是確保藥品質量在整個使用期限內保持穩定,效能與安全不受時間影響。
藥品穩定性測試
在香港,無論是創新藥、仿製藥或生物相類似藥,申請註冊時均須向衞生署提交穩定性數據,這些數據主要來自以下兩種測試方法:
- 長期測試:模擬正常儲存環境,以特定溫度和濕度進行測試,用實時數據支持產品標籤上的儲存溫度及使用期限。
- 加速測試:將藥品放於較極端條件(如攝氏40度高溫/相對濕度75%)進行測試,以較短試驗時間預測長期穩定性。這個測試有助藥廠在研發階段快速篩選合適的配方及包裝方案。
有些藥品對溫度特別敏感,需要存放在雪櫃、冰箱甚至更低溫的環境(例如一些先進療法製品及信使核糖核酸疫苗使用前須儲存於零下60至90度的超低溫環境)。藥廠會採用不同溫濕度組合作出測試,從而制定最適合的儲存方案。
包裝及供應鏈
藥品包裝直接控制藥品的儲存環境,是保持穩定性的關鍵因素。常見的藥品包裝材料包括塑膠、玻璃、鋁箔及複合材料。對於容易受環境影響的藥品,選對包裝物料可減低光照、濕度及溫度的影響,以及與藥物產生化學反應的風險。因此,藥品必須裝載在預備最終上市的包裝內進行穩定性測試,以模擬真實情況。有些容易受潮的藥品,如泡騰片,包裝除了要密封之外,還需内置乾燥劑,以確保藥品保持乾燥。
包裝以外,研究人員也會考慮上市地方的氣候及運輸時的環境變化,以及在整個供應鏈中可能遇到的短期溫度和濕度偏移等狀況,在相應的溫度和濕度下進行測試。
調配或開封後的穩定性
對於需要冲服、溶解或稀釋後使用的藥品,如口服溶液用粉劑、粉針劑和注射用濃縮液等,研究人員還須研究調配後的存放時間、是否需要冷藏等等。這些對患者與照顧者有用的資訊,都必須寫進產品的説明。
大家日後需要服藥的時候,記緊細閱藥品標籤上的儲存說明及有效期,上面都是經過嚴謹科學證明的重要資訊。
香港監管制度與國際接軌
中國香港正積極籌備申請成為 「國際人用藥品註冊技術協調會」(International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use,簡稱ICH)監管機構成員,以推動藥品註冊技術標準與國際接軌,提升香港在藥品監管領域的競爭力和影響力,此舉亦有助年底成立的「香港藥物及醫療器械監督管理中心」長遠發展為國際權威機構。
ICH Q1《穩定性指導原則》為全球藥品穩定性測試提供統一科學標準,而穩定性正是確保藥品安全、有效與質量的關鍵。現時所有在港註冊的藥劑製品,擬定使用期限時均已通過嚴謹的穩定性測試。為配合中國香港爭取成為 ICH 監管機構成員及邁向「第一層審批」的路線圖,由 2026 年 3 月 31 日起,新藥的註冊申請將進一步全面落實 ICH Q1 指導原則,這項要求適用於本地與海外研發的藥劑製品,對藥品穩定性有更全面的要求。衞生署會加強與業界溝通、更新申請指南,方便業界了解詳情。
保障市民健康,實現「好藥港用」,是衞生署堅定不移的使命。通過採納 ICH 等國際權威機構頒布的技術標準,香港的藥物監管體系與生物醫藥產業將更趨穩健,為香港成為全球醫療創新樞紐奠定堅實基礎。