REDWOOD CITY, Calif.--(BUSINESS WIRE)--Mar 25, 2026--
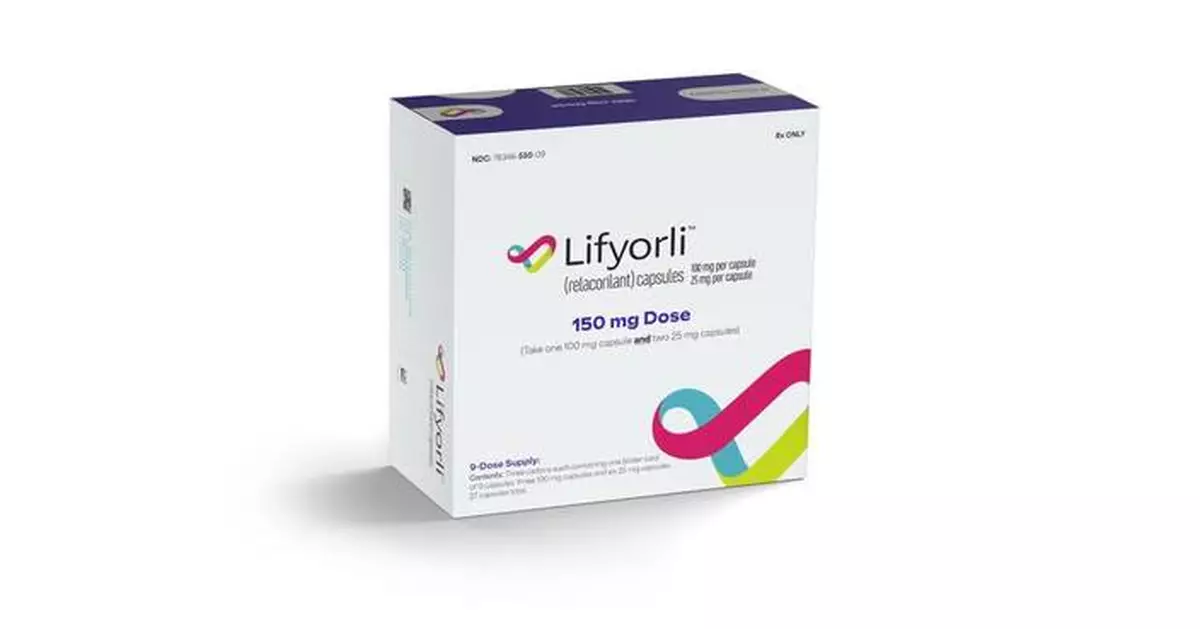
Corcept Therapeutics Incorporated(NASDAQ: CORT)是一家透過調節皮質醇激素作用,從事嚴重內分泌、腫瘤、代謝及神經系統疾病藥物發現與開發的商業階段公司,於今日宣布美國食品藥物管理局(FDA)已批准 Lifyorli™ (relacorilant) 結合 nab-paclitaxel,用於治療已接受一至三線全身性治療方案(其中至少一線包含 bevacizumab)的鉑類抗藥性上皮性卵巢癌、輸卵管癌或原發性腹膜癌成人患者。Lifyorli 是首款獲 FDA 批准的選擇性糖皮質激素受體拮抗劑(SGRA)。

Lifyorli 紙盒 AP圖片
是次批准乃基於 Lifyorli 關鍵性 ROSELLA 試驗的正面結果。該試驗招募了381名曾接受一至三線治療(其中至少一線包含 bevacizumab)的鉑類抗藥性卵巢癌患者。患者以1:1的比例隨機分配,接受 Lifyorli 加 nab-paclitaxel 或單獨使用 nab-paclitaxel 治療。試驗並無要求生物標誌物篩選。
ROSELLA 試驗達到了無惡化存活期及總體存活期的雙重主要終點。與單獨接受 nab-paclitaxel 治療的患者相比,接受 Lifyorli 加 nab-paclitaxel 治療的患者死亡風險降低了35%(風險比:0.65;p值:0.0004),中位總體存活期(OS)為16.0個月,而單獨接受 nab-paclitaxel 治療的患者為11.9個月,兩者相差4.1個月。經盲法獨立中央審查(PFS-BICR)評估,接受 Lifyorli 加 nab-paclitaxel 治療的患者疾病惡化風險亦降低了30%(風險比:0.70;p值:0.008),優於單獨接受 nab-paclitaxel 治療的患者。
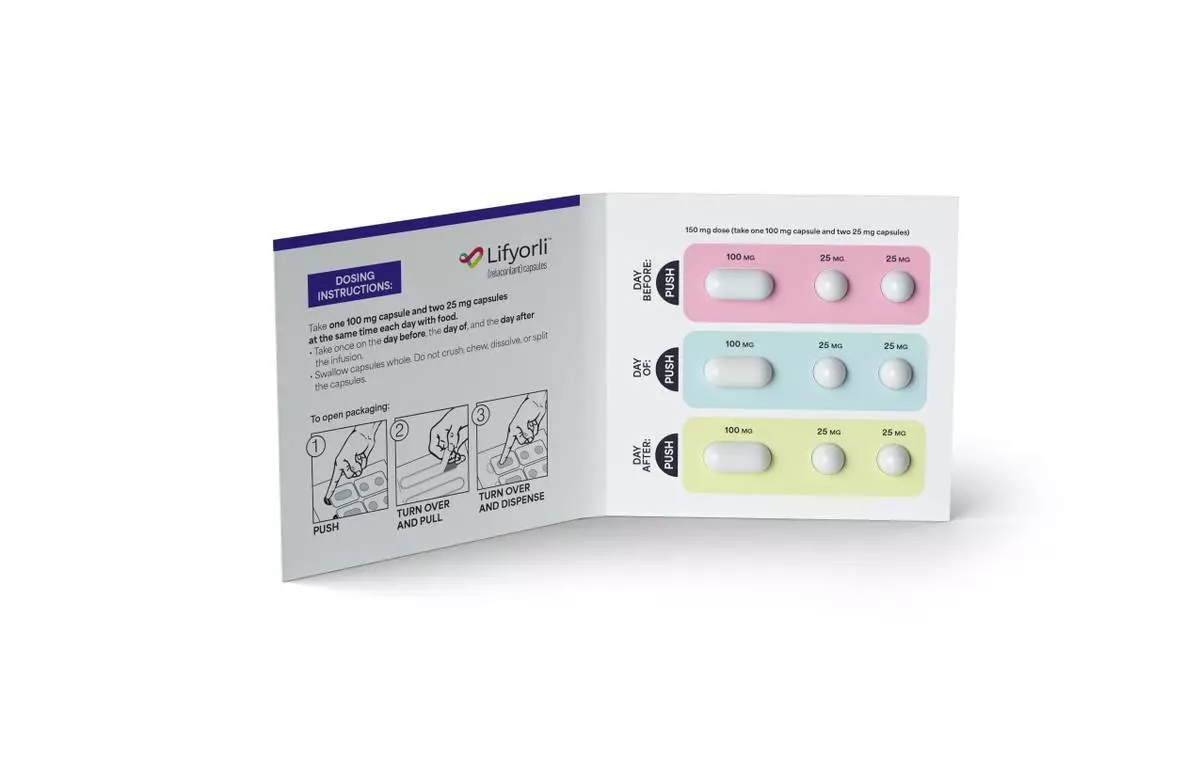
Lifyorli 包裝 AP圖片
Lifyorli 與 nab-paclitaxel 的組合耐受性良好且易於管理。Lifyorli 的安全性是透過 ROSELLA 試驗及 Lifyorli 第二期試驗患者的匯總分析進行評估。Lifyorli 的處方資訊包括中性粒細胞減少症及嚴重感染、腎上腺功能不全、糖皮質激素治療病症惡化以及胚胎-胎兒毒性的警告與注意事項。逾20%患者(包括實驗室異常)最常見的不良反應為血紅蛋白降低、中性粒細胞減少、疲勞、噁心、腹瀉、血小板減少、皮疹及食慾不振。
ROSELLA 試驗的數據首次於 ASCO 2025(美國臨床腫瘤學會)上發表,並同時刊登於《刺針》。ROSELLA 試驗的完整結果將於四月舉行的婦科腫瘤學會(SGO)會議上公布。

Lifyorli 標誌 AP圖片
德州腫瘤學會(Texas Oncology)及 GOG 基金會(GOG Foundation)主席特別顧問羅布科爾曼(Rob Coleman)醫生指出:「數據顯示,Lifyorli 加 nab-paclitaxel 為鉑類抗藥性卵巢癌患者提供了具臨床意義的總體存活期益處,且耐受性良好。Lifyorli 有望成為新的標準治療方案。對於這種晚期復發性疾病,擁有一種新的治療方法將為臨床醫生提供一個引人注目的選擇,以幫助患有這種極難治療癌症的患者。」
卵巢癌研究聯盟(OCRA)首席項目官莎拉迪費奧(Sarah DeFeo)表示:「FDA 批准 Lifyorli 結合 nab-paclitaxel 對於卵巢癌社群的所有人來說都是一個好消息。我們感謝所有參與臨床試驗的患者、他們的家人以及協助推進這種急需治療方案的醫生,為鉑類抗藥性卵巢癌患者帶來希望。」
Corcept 行政總裁約瑟夫貝拉諾夫(Joseph Belanoff)醫生坦言:「能夠為歷史上選擇有限的患者帶來新的治療方法,是我們的榮幸。多年來,我們一直致力於證明皮質醇調節在腫瘤學中的潛力。今日 Lifyorli 獲批是重要的第一步,但這種新的治療模式仍有許多值得探索之處。我們衷心感謝參與臨床試驗的患者和醫療服務提供者,是他們讓這次批准成為可能。」
ROSELLA 試驗在美國、歐洲、南韓、巴西、阿根廷、加拿大及澳洲的試驗點招募了鉑類抗藥性卵巢癌患者,並與 GOG 基金會(GOG-F)、歐洲婦科腫瘤試驗組網絡(ENGOT)、亞太婦科腫瘤試驗組(APGOT)、拉丁美洲合作腫瘤學組(LACOG)及澳洲紐西蘭婦科腫瘤學組(ANZGOG)合作進行。
關於卵巢癌
卵巢癌是女性癌症死亡的第五大常見原因。在接受含鉑治療後六個月內復發的患者被診斷為「鉑類抗藥性」疾病。這些女性的治療選擇很少。在美國,每年約有2萬名鉑類抗藥性疾病患者符合資格開始新的治療,歐洲至少也有相同數量的患者。
關於皮質醇在腫瘤學中的作用
皮質醇透過多種機制在腫瘤生長中發揮作用。它透過抑制細胞凋亡(化療旨在刺激的腫瘤殺傷作用)來幫助實體瘤抵抗化療。在某些癌症中,皮質醇透過激活其結合細胞中的致癌信號來促進腫瘤生長。皮質醇還會抑制身體的免疫反應,削弱其抵抗包括癌症在內的所有疾病的能力。
Corcept 正在開發 relacorilant 用於卵巢癌、子宮內膜癌、宮頸癌、胰腺癌及前列腺癌。Relacorilant 為 Corcept 專有,並受物質組成、使用方法及其他專利保護。它已被歐盟委員會(EC)指定為治療卵巢癌的孤兒藥。Corcept 已向歐洲藥品管理局(EMA)提交了 relacorilant 的上市許可申請(MAA),用於治療鉑類抗藥性卵巢癌患者。
關於 Lifyorli™
Lifyorli (relacorilant) 獲批結合 nab-paclitaxel,是首款獲美國食品藥物管理局(FDA)批准用於治療鉑類抗藥性卵巢癌成人患者的選擇性糖皮質激素受體拮抗劑。Lifyorli 是一種口服藥物,在接受 nab-paclitaxel 治療的前一天、當天及後一天服用。Lifyorli 並無生物標誌物要求。Lifyorli 競爭性地結合糖皮質激素受體(GR),透過抑制皮質醇對細胞凋亡(nab-paclitaxel 等化療旨在引起的程序性細胞死亡)的抑制作用,從而增強化療敏感性。Lifyorli 對身體的其他類固醇受體沒有任何作用。
LIFYORLI 適應症及用法
LIFYORLI 結合 nab-paclitaxel 適用於治療已接受1-3線全身性治療方案(其中至少一線包含 bevacizumab)的鉑類抗藥性上皮性卵巢癌、輸卵管癌或原發性腹膜癌成人患者。
重要安全資訊
禁忌症:
LIFYORLI 禁忌用於接受全身性糖皮質激素以維持生命(例如器官移植後的免疫抑制)的患者,因為 LIFYORLI 會拮抗糖皮質激素的作用。
警告及注意事項:
中性粒細胞減少症及嚴重感染
LIFYORLI 結合 nab-paclitaxel 可能導致中性粒細胞減少症,包括發熱性中性粒細胞減少症及嚴重感染。曾有一宗因發熱性中性粒細胞減少症導致敗血性休克致死的個案。38%的患者在治療的第一或第二個週期內開始使用粒細胞集落刺激因子(G-CSF)。
在每次 LIFYORLI 結合 nab-paclitaxel 的每週治療前及臨床需要時,監測全血細胞計數。根據中性粒細胞減少症的嚴重程度,延遲劑量、減少劑量或永久停用 LIFYORLI 結合 nab-paclitaxel。酌情考慮使用短效 G-CSF。考慮同時存在腎上腺功能不全的可能性,尤其是在嚴重感染的情況下。
腎上腺功能不全
LIFYORLI 是一種可逆的糖皮質激素受體拮抗劑,可能導致腎上腺功能不全。腎上腺功能不全可能在 LIFYORLI 治療期間的任何時候發生。在壓力情況下,例如急性疾病、感染或手術,腎上腺功能不全的風險會增加。對於在手術前30天內接受過 LIFYORLI 的患者,應考慮在圍手術期是否需要補充糖皮質激素。監測接受 LIFYORLI 治療的患者是否有腎上腺功能不全的體徵和症狀。如果懷疑腎上腺功能不全,應暫停 LIFYORLI 並給予糖皮質激素治療。可能需要高劑量的補充糖皮質激素來克服 LIFYORLI 產生的糖皮質激素受體拮抗作用。在腎上腺功能不全解決後,根據嚴重程度恢復先前劑量、減少劑量或永久停用 LIFYORLI。
糖皮質激素治療病症惡化
在服用全身性糖皮質激素治療其他疾病(例如自身免疫性疾病)的患者中使用 LIFYORLI,可能會使這些疾病惡化。LIFYORLI 是一種糖皮質激素受體拮抗劑,可能會降低全身性糖皮質激素的效力。同樣,全身性糖皮質激素的共同給藥可能會降低 LIFYORLI 的效力。監測同時接受 LIFYORLI 和糖皮質激素治療的患者,以防兩者效力降低。
胚胎-胎兒毒性
LIFYORLI 在孕婦中使用可能對胎兒造成傷害。告知孕婦對胎兒的潛在風險。在開始 LIFYORLI 治療前,核實有生育潛力女性的懷孕狀況。建議有生育潛力的女性,包括有生育潛力女性伴侶的男性患者,在 LIFYORLI 治療期間及最後一劑後1週內使用有效避孕措施。
不良反應:
35%接受 LIFYORLI 結合 nab-paclitaxel 治療的患者出現嚴重不良反應。患者中嚴重不良反應(≥2%)包括中性粒細胞減少症(4%)、肺炎(3.2%)、胸腔積液(3.2%)、發熱性中性粒細胞減少症(2.1%)及疲勞(2.1%)。患者中致命不良反應(2.1%)包括敗血性休克(0.5%)、心臟驟停(0.5%)、缺血性中風(0.5%)及腸穿孔(0.5%)。
9%的患者因不良反應而永久停用 LIFYORLI 結合 nab-paclitaxel。導致患者永久停用 LIFYORLI 的不良反應(>2%)是腸梗阻(2.6%)。72%的患者因不良反應而暫停 LIFYORLI 劑量。需要暫停 LIFYORLI 結合 nab-paclitaxel 劑量的不良反應(≥5%)包括中性粒細胞減少症(44%)、貧血(12%)及疲勞(7%)。需要減少 LIFYORLI 劑量的不良反應包括疲勞(1.6%)、食慾不振(1.2%)、腹痛(0.5%)、中性粒細胞減少症(0.5%)、水腫(0.5%)及坐骨神經痛(0.5%)。當 nab-paclitaxel 暫停或停用時,LIFYORLI 亦應暫停或停用。
接受 LIFYORLI 加 nab-paclitaxel 治療的患者最常見的不良反應(>20%),包括實驗室異常,為血紅蛋白降低、中性粒細胞減少、疲勞、噁心、腹瀉、血小板減少、皮疹及食慾不振。
藥物相互作用:
特定人群使用:
請參閱完整的《處方資訊》以獲取更多重要安全資訊。
關於 Corcept Therapeutics
逾25年來,Corcept 一直專注於皮質醇調節及其治療多種嚴重疾病的潛力,並已發現逾1,000種專有的選擇性皮質醇調節劑及糖皮質激素受體拮抗劑。Corcept 正在對庫欣綜合症、實體瘤、肌萎縮性脊髓側索硬化症(ALS)及肝病患者進行高級臨床試驗。2012年,該公司推出了 Korlym ®,這是首款獲美國食品藥物管理局(FDA)批准用於治療內源性庫欣綜合症患者的藥物;2026年,該公司推出了 Lifyorli™,獲批結合 nab-paclitaxel,是首款獲 FDA 批准用於治療鉑類抗藥性卵巢癌成人患者的選擇性糖皮質激素受體拮抗劑。Corcept 總部位於加州紅木城。
前瞻性陳述
本新聞稿中除歷史事實陳述外的所有陳述均為前瞻性陳述,基於我們目前的計劃和預期,並受風險和不確定性的影響,可能導致我們的實際結果與此類前瞻性陳述所表達或暗示的任何未來結果存在重大差異。
在本新聞稿中,前瞻性陳述包括以下內容:Lifyorli 的療效、安全性概況及其他臨床特性,以及其成為鉑類抗藥性卵巢癌患者新標準治療方案的潛力,並為臨床醫生提供一個引人注目的選擇,以幫助患有這種難治性癌症的患者;ROSELLA 試驗的完整結果將在 SGO 會議上公布;我們證明皮質醇調節在腫瘤學中的潛力並進一步探索這種治療模式的能力;我們在卵巢癌、子宮內膜癌、宮頸癌、胰腺癌及前列腺癌中進一步開發 relacorilant 的情況;預計每年在美國和歐洲開始新治療的鉑類抗藥性卵巢癌患者的發生率;以及我們對 Lifyorli 及時讓患者使用的承諾。
有關風險和不確定性的進一步描述可在我們的美國證券交易委員會(SEC)文件(可在我們的網站和 SEC 網站上查閱)中找到。這些風險和不確定性包括但不限於:我們經營業務的能力;我們研究和開發 Korlym、relacorilant、miricorilant、dazucorilant、nenocorilant 及我們其他候選產品的努力;這些分子的臨床特性;監管機構對我們的產品或業務施加的批准、指令、監督及其他法律、法規或政府機關酌情權要求;以及我們知識產權的範圍和保護力。我們不承擔更新本新聞稿中前瞻性陳述的任何意圖或義務。
(美聯社)