加州聖塔菲泉 2026年4月8日電
布萊恩實驗室公司(Blaine Labs, Inc.)宣布自願回收三批次的傷口護理凝膠(Wound Care Gel)產品,包括1安士及3安士裝(含0.1%苯扎氯銨),原因為產品受微生物污染。
Tridergel™ 傷口護理凝膠 - 1安士長尖頭瓶裝 AP圖片
受影響產品被驗出含有梭狀芽孢桿菌(Lysinibacillus fusiformis),這是一種環境微生物。
風險聲明
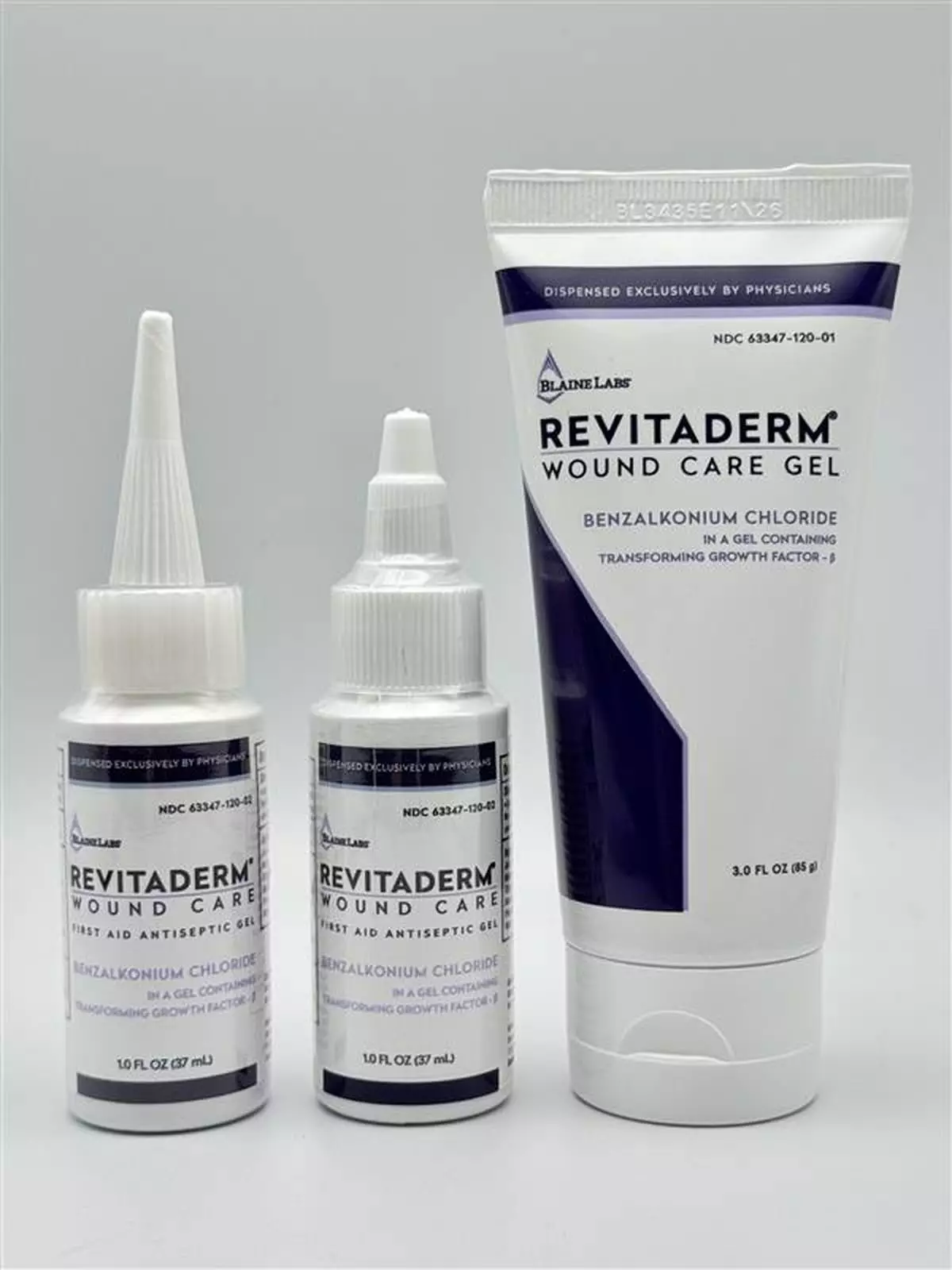
Revitaderm® 傷口護理凝膠 - (從左至右)1安士長尖頭瓶裝、1安士短旋轉蓋瓶裝及3安士管裝 AP圖片
是次自願回收是預防性措施,因產品檢測到微生物存在。經測試樣本確認含有梭狀芽孢桿菌。梭狀芽孢桿菌是一種環境中的孢子形成細菌。
雖然該菌對健康人士的致病性普遍較低,但它能在惡劣環境中存活,並可能成為機會性病原體。開放性傷口、皮膚屏障受損或免疫系統較弱的患者(例如長者、糖尿病患者或免疫功能受損人士)可能面臨更高的感染、皮膚刺激及/或傷口癒合延遲風險。對於免疫功能受損人士,包括糖尿病控制不佳者、免疫衰老的長者,以及免疫系統未成熟的幼童,這些感染可能變得嚴重,並導致危及生命的併發症,例如心內膜炎或中樞神經系統感染。
該產品用作局部消毒劑,用於急救,以幫助預防輕微割傷、擦傷和燒傷的感染風險。產品以1安士瓶裝和3安士管裝出售。Revitaderm® 傷口護理凝膠可透過其紫色邊飾識別,而Tridergel™ 傷口護理則可透過其淺藍色邊飾識別。1安士瓶裝有兩種瓶蓋配置:旋轉蓋和較長的尖頭蓋,並以收縮帶/瓶身帶密封。瓶底印有有效日期和批號。3安士管裝的批號和有效日期則印在管頂的壓邊處。Revitaderm® 傷口護理消毒凝膠(1安士及3安士)和Tridergel™ 傷口護理(1安士)已在美國全國範圍內分銷給醫療服務提供者(診所),並未分銷作零售或網上銷售。
截至目前,布萊恩實驗室公司尚未收到任何與是次回收相關的不良事件報告。
客戶應如何處理
客戶及醫療服務提供者應檢查其庫存中是否有這些受影響批號的產品,並立即停止使用及/或分銷。請立即停止使用產品。將這些批號的剩餘庫存隔離,並請聯絡布萊恩實驗室公司安排退貨。
布萊恩實驗室公司正透過普通郵件及電話(如適用)通知其醫生診所,並正安排回收與是次回收相關批號中未分發的1安士和3安士產品。
消費者如有關於是次回收的疑問,可於周一至周五上午7時30分至下午4時(太平洋夏令時間),直接透過以下聯絡資訊聯絡布萊恩實驗室公司。
您亦可使用以下聯絡資訊,直接向布萊恩實驗室公司報告不良事件或關於是次回收的疑問。
使用本產品時出現的不良反應或品質問題,可透過網上、普通郵件或傳真方式,向美國食品藥物管理局(FDA)的MedWatch不良事件通報計劃報告。
是次回收是在美國食品藥物管理局的知情下進行。
(美聯社)
全球數碼健康公司 Glooko 今日宣布,其 EndoTool IV Cloud 平台已獲美國食品藥物管理局(FDA)授予 510(k) 批准。該平台是首個獲 FDA 批准、以雲端為基礎、針對個別病人的胰島素劑量平台。Glooko 致力協助臨床醫生應對血糖安全及糖尿病管理日益嚴峻的挑戰。EndoTool IV Cloud 是 Glooko 旗下 EndoTool IV 的雲端版本,為醫院環境中的靜脈注射胰島素劑量提供臨床決策支援。
EndoTool IV 獲醫院採用,以支援需要靜脈注射胰島素治療的住院病人,提供個別化的胰島素劑量。EndoTool IV Cloud 沿用 EndoTool IV 相同的可靠臨床基礎,將該方案經驗證的胰島素劑量功能引入雲端環境,支援更具擴展性的實施、精簡的維護及未來的平台創新。

(Glooko 圖片) Glooko 宣布 EndoTool IV Cloud 獲 FDA 510(k) 批准。 AP圖片
是次批准標誌著 Glooko 在推動住院及門診環境中互聯糖尿病護理策略的重要里程碑。
Glooko 行政總裁邁克·阿爾瓦雷斯(Mike Alvarez)表示:「EndoTool IV Cloud 獲 FDA 510(k) 批准,對 Glooko、我們的醫院客戶以及互聯糖尿病護理的未來而言,是重要一步。EndoTool IV 已是住院胰島素劑量的可靠方案。透過將其針對個別病人的劑量功能引入雲端平台,我們不僅是邁向雲端,更協助樹立醫院如何擴展血糖安全及個別化護理的新標準。」
EndoTool IV Cloud 採用與現有 EndoTool IV 方案相同的核心胰島素劑量演算法,同時引入雲端功能,預計將支援更高效的部署、集中式更新及更靈活的平台架構。該雲端模式旨在減少對內部部署基礎設施的需求,並為採用或擴展使用 EndoTool IV 的醫院提供更具擴展性的方法。
Glooko 旗下 EndoTool 醫學總監保羅·奇德斯特醫生(Paul Chidester, M.D.)指出:「EndoTool 在協助醫院管理靜脈注射胰島素治療方面,已展現強大的臨床價值,包括降低低血糖風險、更快達到目標血糖水平、改善血糖達標時間,以及減少所需的血糖檢查。透過 EndoTool IV Cloud,我們保留了相同的可靠臨床基礎及胰島素劑量演算法,同時使該方案更易於醫院團隊部署、維護及擴展。」
EndoTool IV Cloud 的推出,反映 Glooko 自 2025 年 9 月收購 Monarch Medical Technologies 後,對 EndoTool 平台的持續投資。Glooko 正準備商業發布,並與其團隊及客戶緊密合作,為現有 EndoTool IV 內部部署用戶提供周全的過渡策略。現有 EndoTool IV 客戶將繼續獲得支援,Glooko 將在 EndoTool IV Cloud 商業上市時,提供指導、培訓及過渡資源。
Glooko 互聯護理總裁里奇·格倫(Rich Glenn)表示:「EndoTool IV Cloud 代表我們住院胰島素劑量平台的下一個演進。透過這個里程碑,我們將 EndoTool IV 推進到雲端環境,旨在為醫院提供更具擴展性、靈活性及效率的方式來部署及管理該方案。隨著我們準備在今年稍後時間進行商業發布,我們的重點是為客戶提供周全的體驗,同時為整個醫療系統的長期創新及價值奠定更堅實的基礎。」
EndoTool IV Cloud 預計將於今年年底前在美國商業發布。
EndoTool IV 是一款臨床決策支援方案,旨在支援醫院環境中的個別化靜脈注射胰島素劑量。該方案利用針對個別病人的數據,建議胰島素劑量調整,並協助臨床醫生為需要靜脈注射胰島素治療的病人管理血糖控制。
EndoTool IV Cloud 採用與現有 EndoTool IV 方案相同的胰島素劑量演算法,將此功能引入雲端環境。
Glooko 是一家全球數碼健康公司,致力協助臨床醫生應對血糖安全及糖尿病管理日益嚴峻的挑戰。Glooko 獨特地定位為醫療服務提供者的首選企業合作夥伴,旨在降低血糖風險、提高安全性,並透過在門診及住院護理環境中協調專業知識,支援負擔過重的臨床團隊。
EndoTool 由 Glooko 旗下公司 Monarch Medical Technologies 有限責任公司開發及銷售,是獨立於 Glooko 糖尿病管理平台之外的方案。EndoTool 是一款獲 FDA 批准的第二類醫療設備,適用於其使用說明中描述的住院用途。所有建議旨在輔助而非取代臨床判斷。
(美聯社)